Свойства периодической системы менделеева – Периодическая таблица химических элементов – это… Что такое Периодическая таблица химических элементов?
- Комментариев к записи Свойства периодической системы менделеева – Периодическая таблица химических элементов – это… Что такое Периодическая таблица химических элементов? нет
- Советы абитуриенту
- Периодический закон и система Д.И. Менделеева
- Структура периодической системы Менделеева
- Структура периодической системы
- Периодический закон и периодическая система Менделеева
- Периодическая система Менделеева и периодический закон
- ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ | Энциклопедия Кругосвет
- Классификации по «атомному весу»
- Гипотеза Праута.
- Триады Доберейнера.
- Октавы Ньюлендса.
- Периодический закон.
- Периодическая таблица.
- Периоды.
- Группы и подгруппы.
- Металлы, неметаллы.
- Валентность.
- Физический смысл атомного номера.
- Строение атома.
- Определение понятия атомного номера.
- Периодичность и атомная структура.
- Электронные конфигурации.
- Короткие и длинные периоды.
- Лантаноиды и актиноиды.
- Применение периодической таблицы.
- Периодическая система Менделеева • Джеймс Трефил, энциклопедия «Двести законов мироздания»
Периодический закон и система Д.И. Менделеева
1. Слева направо по периоду (см. Таблица Менделеева):
-
- металлические свойства простых веществ ослабевают (уменьшаются)
- неметаллические свойства усиливаются (увеличиваются)
- радиус атома уменьшается (атомное сжатие из-за увеличения заряда ядра)
- электроотрицательность элементов возрастает (самый ЭО элемент – фтор)
- восстановительные свойства уменьшаются
- окислительные свойства увеличиваются
- основные свойства оксидов и гидроксидов уменьшаются
- Кислотные свойства оксидов и гидроксидовусиливаются
- идет увеличение числа электронов на внешнем уровне
- увеличивается максимальная валентность элементов
2. Сверху вниз по группе (см. Таблица Менделеева) (для главной подгруппы):
-
- металлические свойства простых веществ усиливаются
- неметаллические свойства ослабевают
- радиус атома увеличивается
- электроотрицательность элементов уменьшается
- основные свойства оксидов и гидроксидов усиливаются
- кислотные свойства оксидов и гидроксидов убывают
- Число электронов на внешнем уровне не меняется
3. К основным оксидам относятся оксиды металлов со степенью окисления +1 и +2
4. К кислотным оксидам относятся оксиды неметаллов и оксиды металлов со степенью окисления +5, +6, +7
5. К амфотерным оксидам относятся Al2O3, BeO, ZnO, Cr2O3
Давайте порассуждаем вместе
1. Как изменяется радиус атома в ряду Be – Mg – Ca ?
1) уменьшается
2) увеличивается
3) не изменяется4) сначала уменьшается, потом увеличивается
Ответ: все элементы находятся в одной группе, сверху вниз, значит радиус атома увеличивается
2. Как изменяются металлические свойства в ряду Li – Be – B?
1) не изменяются
2) сначала усиливаются, потом уменьшаются
3) ослабевают
4) усиливаются
Ответ: все элементы находятся в одном периоде слева направо, значит металлические свойства ослабевают
3. Как изменяется электроотрицательность в ряду F – O – N?
1) сначала усиливается, потом ослабевает
2) уменьшается
3) не изменяется
4) усиливается
Ответ: все элементы находятся в одном периоде справа налево, значит электроотрицательность уменьшается.
4. Как изменяются неметаллические свойства в ряду As – P – N?
1) уменьшаются
2) не изменяются
3) сначала усиливаются, потом уменьшаются
4) усиливаются
Ответ: все элементы находятся в одной группе снизу вверх, значит неметаллические свойства усиливаются
5. Как изменяется число валентных электронов в ряду Li – Na – K?
1) не изменяется
2) увеличивается
3) уменьшается
4) сначала уменьшается, затем увеличивается
Ответ: все элементы находятся в одной группе сверху вниз, значит число валентных электронов не изменяется
6. Как изменяются окислительные свойства в ряду O – S – Se?
1) увеличиваются
2) сначала уменьшаются, затем увеличиваются
3) не изменяются
4) уменьшаются
Ответ: все элементы находятся в одной группе сверху вниз, значит окислительные свойства уменьшаются
7. Как изменяются восстановительные свойства в ряду Si – Al – Mg?
1) сначала уменьшаются, затем усиливаются
2) увеличиваются
3) не изменяются
4) уменьшаются
Ответ: все элементы находятся в одном периоде справа налево, значит восстановительные свойства усиливаются
8. Как изменяются свойства оксидов в ряду MgO -> Al
1) от основных к кислотным
2) от кислотных к основным
3) от кислотных к амфотерным
4) от основных к амфотерным
Ответ: все элементы находятся в одном периоде слева направо, значит свойства оксидов изменяются от основных к кислотным
Задания повышенной сложности
1. В главных подгруппах периодической системы с увеличением заряда ядра атомов химических элементов происходит:
1) усиление неметаллических свойств
2) усиление металлических свойств
3) высшая валентность элементов остается постоянной
4) изменяется валентность в водородных соединениях
5) уменьшается радиус атомов
Ответ: 2, 3
2. В главных подгруппах периодической системы восстановительная способность атомов увеличивается по мере
1) уменьшения радиуса атома
2) увеличения числа электронных слоев в атомах
3) уменьшения заряда ядра атомов
4) увеличения числа валентных электронов
5) увеличения порядкового номера элемента
Ответ: 2, 5
3. В ряду химических элементов Be, Mg, Ca, Sr
1) усиливается способность атомов отдавать электроны
2) уменьшается заряд ядра атомов
3) усиливается восстановительная способность
4) уменьшаются металлические свойства
5) усиливается способность атомов принимать электроны
Ответ: 1, 3
4. В ряду химических элементов I, Br, Cl, F восстановительная способность атомов уменьшается, потому что
1) увеличивается радиус атома
2) увеличивается заряд ядра атомов
3) увеличивается число электронных слоев в атомах
4) уменьшается число электронных слоев в атомах
5) уменьшается способность атомов отдавать электроны
Ответ: 4, 5
5. В ряду химических элементов As, P, N
1) увеличивается радиус атома
2) увеличивается электроотрицательность
3) усиливаются кислотные свойства их высших оксидов
4) возрастает значение высшей степени окисления5) увеличивается число электронов во внешнем электронном слое атомов
Ответ: 2, 3
6. В ряду химических элементов P, N, O
1) уменьшается число электронов во внешнем электронном слое
2) увеличивается электроотрицательность
3) возрастает значение высшей валентности
4) ослабевают неметаллические свойства
5) усиливается способность атомов принимать электроны
Ответ: 2, 5
7. В ряду гидроксидов NaOH, Ca(OH)2, Al(OH)3
1) увеличивается термическая стойкость
2) ослабевают основные свойства
3) увеличивается способность к электролитической диссоциации
4) ослабевают окислительные свойства
5) уменьшается растворимость в воде
Ответ: 2,5
dx-dy.ru
Структура периодической системы Менделеева
Анализируя данные о внутренней связи между группами сходных по свойствам элементов, Д. И. Менделеев пришел к выводу, что их свойства должны быть обусловлены какими-то фундаментальными общими характеристиками. Такой фундаментальной характеристикой для химического элемента он выбрал атомную массу элемента и кратко сформулировал периодический закон (1869 г.):
Свойства элементов, а также свойства образуемых ими простых и сложных тел находятся в периодической зависимости от величин атомных весов элементов.
Заслуга Менделеева состоит в том, что он понял проявленную зависимость как объективную закономерность природы, чего не смогли сделать его предшественники. Д. И. Менделеев считал, что в периодической зависимости от атомной массы находятся состав соединений, их химические свойства, температуры кипения и плавления, строение кристаллов и тому подобное. Глубокое понимание сути периодической зависимости дало Менделееву возможность сделать несколько важных выводов и предположений.
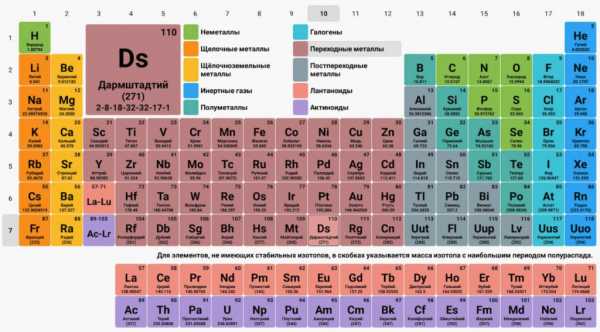 Современная таблица Менделеева
Современная таблица МенделееваВо-первых, из известных в то время 63 элементов Менделеев изменил атомные массы почти у 20 элементов (Be, In, La, Y, Ce, Th, U). Во-вторых, он предсказал существование около 20 новых элементов и оставил для них место в периодической системе. Три из них, а именно экабор, екаалюминий и екасилиций были описаны достаточно подробно и с удивительной точностью. Это триумфально подтвердилось в течение последующих пятнадцати лет, когда были открыты элементы Галлий (екаалюминий), скандий (экабор) и Германий (екасилиций).
Периодический закон является одним из фундаментальных законов природы. Его влияние на развитие научного мировоззрения можно сравнить только с законом сохранения массы и энергии или квантовой теории. Еще во времена Д. И. Менделеева периодический закон стал основой химии. Дальнейшие открытия строения атома и явления изотопии показали, что главной количественной характеристикой элемента является не атомная масса, а заряд ядра(Z). В 1913 г. Мозли и Резерфорд ввели понятие «порядковый номер элемента», пронумеровали в периодической системе все символы и показали, что в основу классификации элементов является порядковый номер элемента, равный заряда ядер их атомов.
Это утверждение известно сейчас как закон Мозли.
Поэтому современное определение периодического закона формулируется следующим образом:
Свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от значения заряда их атомных ядер (или от порядкового номера элемента в периодической системе).
Электронные структуры атомов элементов наглядно показывают, что при росте заряда ядра происходит закономерное периодическое повторение электронных структур, а значит, и повторение свойств элементов. Это отражается в периодической системе элементов, для которой предложено несколько сотен вариантов. Чаще всего используют две формы таблиц — сокращенную и развернутую, — содержащие все известные элементы и имеющие свободные места для пока не открытых.
Каждый элемент занимает в периодической таблице определенную ячейку, в которой указано символ и название элемента, его порядковый номер, относительную атомную массу, а для радиоактивных элементов в квадратных скобках приведены массовое число наиболее стабильного или доступного изотопа. В современных таблицах часто приводятся и некоторые другие справочные сведения: плотность, температуры кипения и плавления простых веществ и т.п.
Периоды
Основными структурными единицами периодической системы есть периоды и группы — естественные совокупности, на которые делятся химические элементы по электронным структурами.
Период — это горизонтальный последовательный ряд элементов, в атомах которых электроны заполняют одинаковое количество энергетических уровней.
Номер периода совпадает с номером внешнего квантового уровня. Например, элемент кальций ( 4s2 ) находится в четвертом периоде, то есть его атом имеет четыре энергетические уровни, а валентные электроны находятся на внешнем, четвертом уровне. Разница в последовательности заполнения как внешних, так и более близких к ядру электронных слоев объясняет причину различной длины периодов.
В атомов s- и р-элементов идет застройка внешнего уровня, в d-элементов — второго снаружи, а в f-элементов — третьего снаружи энергетического уровня.
Поэтому различие в свойствах наиболее отчетливо проявляется в соседних s- или р-элементах. В d- и особенно f-элементах одного и того же периода различие в свойствах менее значительно.
Как уже упоминалось, по признаку номера энергетического подуровня застраиваемого электронами, элементы объединяются в электронные семьи. Например, в IV-VI периодах находятся семьи, которые содержат по десять d-элементов: 3d-семья (Sc-Zn), 4d- семья (Y-Cd), 5d- семья (La, Hf-Hg). В шестом и седьмом периодах по четырнадцать элементов составляют f-семьи: 4f-семью (Се-Lu), которая носит название лантаноидной, и 5f-семью (Th-Lr) — актиноидную. Эти семьи размещают под периодической таблицей.
Первые три периода называются малыми, или типичными периодами, поскольку свойства элементов этих периодов является основой для распределения всех других элементов на восемь групп. Все остальные периоды, включая и седьмой, незавершенный, называются большими периодами .
Все периоды, кроме первого, начинаются с щелочных металлов (Li, Na, K, Rb, Cs, Fr) и заканчиваются, за исключением седьмого, незавершенного, инертными элементами (He, Ne, Ar, Kr, Xe, Rn). Щелочные металлы имеют одну и ту же внешнюю электронную конфигурацию ns1 , где n — номер периода. Инертные элементы, кроме гелия ( 1s2 ), имеют одинаковое строение внешнего электронного слоя: ns2 np6 , то есть электронными аналогами.
Рассмотренная закономерность дает возможность прийти к выводу:
Периодическое повторение одинаковых электронных конфигураций внешнего электронного слоя является причиной сходства физических и химических свойств у элементов-аналогов, так как именно внешние электроны атомов в основном определяют их свойства .
В малых типовых периодах с увеличением порядкового номера наблюдается постепенное уменьшение металлических и рост неметаллических свойств, поскольку увеличивается количество валентных электронов на внешнем энергетическом уровне. Например, атомы всех элементов третьего периода имеют по три электронных слоя. Строение двух внутренних слоев одинаково для всех элементов третьего периода (1s2 2s2 2p6), а строение внешнего, третьего, слоя различно. При переходе от каждого предыдущего элемента к каждому последующему заряд ядра атома возрастает на единицу и соответственно увеличивается количество внешних электронов. В результате их притяжение к ядру усиливается, а радиус атома уменьшается. Это приводит к ослаблению металлических свойств и росту неметаллических.
Третий период начинается очень активным металлом натрием ( 11Na — 3s1 ), за которым следует несколько менее активный магний ( 12Mg — 3s2 ). Оба эти металлы относятся к 3s-семье. Первый р-элемент третьего периода алюминий ( 13Al — 3s2 3p1 ), металлическая активность которого меньше, чем у магния, имеет амфотерные свойства, то есть в химических реакциях может вести себя и как неметалл. Далее следуют неметаллы кремний ( 14Si — 3s2 3p2 ), фосфор ( 15P — 3s2 3p3 ), сера ( 16S — 3s2 3p4 ), хлор ( 17Cl — 3s2 3p5 ). Их неметаллические свойства усиливаются от Si к Cl, который является активным неметаллом. Период заканчивается инертным элементом аргоном ( 18Ar — 3s2 3p6 ).
В пределах одного периода свойства элементов меняются постепенно, а при переходе от предыдущего периода к следующему наблюдается резкое изменение свойств, поскольку начинается застройка нового энергетического уровня.
Постепенность изменения свойств характерна не только для простых веществ, но и для сложных соединений, как это представлено в таблице 1.
Таблица 1 — Некоторые свойства элементов третьего периода и их соединений
| Электронная семья | s-элементы | р-элементы | ||||||
|---|---|---|---|---|---|---|---|---|
| Символ элемента | Na | Mg | Al | Si | P | S | Cl | Ar |
| Заряд ядра атома | +11 | +12 | +13 | +14 | +15 | +16 | +17 | +18 |
| Внешняя электронная конфигурация | 3s 1 | 3s 2 | 3s 2 3p 1 | 3s 2 3p2 | 3s 2 3p 3 | 3s 2 3p 4 | 3s 2 3p 5 | 3s 2 3p 6 |
| Атомный радиус, нм | 0,189 | 0,160 | 0,143 | 0,118 | 0,110 | 0,102 | 0,099 | 0,054 |
| Максимальная валентность | I | II | III | IV | V | VI | VII | — |
| Высшие оксиды и их свойства | Na 2 O | MgO | Al 2 O 3 | SiO 2 | P 2 O 5 | SO 3 | Cl 2 O 7 | — |
| Основные свойства | Амфотерные свойства | Кислотные свойства | — | |||||
| Гидраты оксидов (основы или кислоты) | NaOH | Mg (OH) 2 | Al (OH) 3 | H 2 SiO 3 | H 3 PO 4 | H 2 SO 4 | HСlO 4 | — |
| Основание | Слабое основание | Амфотерный гидроксид | Слабая кислота | Кислота средней силы | Сильная кислота | Сильная кислота | — | |
| Соединения с водородом | NaH | MgH 2 | AlH 3 | SiH 4 | PH 3 | H 2 S | HCl | — |
| Твердые солеобразные вещества | Газообразные вещества | — | ||||||
В больших периодах металлические свойства ослабляются медленнее. Это связано с тем, что, начиная с четвертого периода, появляются десять переходных d-элементов, в которых застраивается не внешний, а второй снаружи d-подуровень, а на внешнем слое d-элементов находятся один или два s-электрона, которые и определяют в известной степени свойства этих элементов. Таким образом, для d-элементов закономерность несколько усложняется. Например, в пятом периоде металлические свойства постепенно уменьшаются от щелочного Rb, достигают минимальной силы у металлов семьи платины (Ru, Rh, Pd).
Однако после неактивного Ag серебра размещается кадмий Cd, у которого наблюдается скачкообразный рост металлических свойств. Далее с ростом порядкового номера элемента появляются и постепенно усиливаются неметаллические свойства вплоть до типового неметалла йода. Заканчивается этот период, как и все предыдущие, инертным газом. Периодическая смена свойств элементов внутри больших периодов позволяет разделить их на два ряда, в которых вторая часть периода повторяет первую.
Группы
Вертикальные столбики элементов в периодической таблице — группы состоят из подгрупп: главной и побочной, они иногда обозначаются буквами А и Б соответственно.
В состав главных подгрупп входят s- и р-элементы, а в состав побочных — d- и f-элементы больших периодов.
Главная подгруппа — это совокупность элементов, которая размещается в периодической таблице вертикально и имеет одинаковую конфигурацию внешнего электронного слоя в атомах.
Как следует из приведенного определения, положения элемента в главной подгруппе определяется общим количеством электронов (s- и р-) внешнего энергетического уровня, равным номеру группы. Например, сера (S — 3s2 3p4 ), в атоме которого на внешнем уровне содержится шесть электронов, относится к главной подгруппе шестой группы, аргон (Ar — 3s2 3p6 ) — к главной подгруппе восьмой группы, а стронций (Sr — 5s2 ) — к ІІА-подгруппе.
Элементы одной подгруппы характеризуются сходством химических свойств. В качестве примера рассмотрим элементы ІА и VІІА подгрупп (табл.2). С ростом заряда ядра увеличивается количество электронных слоев и радиус атома, но количество электронов на внешнем энергетическом уровне остается постоянной: для щелочных металлов (подгруппа IА) — один, а для галогенов (подгруппа VIIА) — семь. Поскольку именно внешние электроны наиболее существенно влияют на химические свойства, то понятно, что каждая из рассмотренных групп элементов-аналогов имеет подобные свойства.
Но в пределах одной подгруппы наряду с подобием свойств наблюдается их некоторое изменение. Так, элементы подгруппы ІА все, кроме Н — активные металлы. Но с ростом радиуса атома и количества электронных слоев экранирующих влияние ядра на валентные электроны, металлические свойства усиливаются. Поэтому Fr более активный металл, чем Сs, a Cs — более активный, чем R в и т.д. А в подгруппе VIIA по той же причине ослабляются неметаллические свойства элементов при росте порядкового номера. Поэтому F — более активный неметалл по сравнению с Cl, a Cl — более активный неметалл сравнению с Br и т.д.
Таблица 2 — Некоторые характеристики элементов ІА и VІІА-подгрупп
| период | Подгруппа IA | Подгруппа VIIA | ||||||
|---|---|---|---|---|---|---|---|---|
| Символ элемента | Заряд ядра | Радиус атома, нм | Внешняя электронная конфигурацiя | Символ элемента | Заряд ядра | Радиус атома, нм | Внешняя электронная конфигурацiя | |
| II | Li | +3 | 0,155 | 2 s 1 | F | +9 | 0,064 | 2 s 2 2 p 5 |
| III | Na | +11 | 0,189 | 3 s 1 | Cl | +17 | 0,099 | 3 s 2 3 p 5 |
| IV | K | +19 | 0,236 | 4 s 1 | Br | 35 | 0,114 | 4 s 2 4 p 5 |
| V | Rb | +37 | 0,248 | 5 s 1 | I | +53 | 0,133 | 5 s 2 5 p 5 |
| VI | Cs | 55 | 0,268 | 6 s 1 | At | 85 | 0,140 | 6 s 2 6 p 5 |
| VII | Fr | +87 | 0,280 | 7 s 1 | — | — | — | — |
Побочные подгруппа — это совокупность элементов, размещаемых в периодической таблице вертикально и имеют одинаковое количество валентных электронов за счет застройки внешнего s- и втором снаружи d-энергетических подуровней.
Все элементы побочных подгрупп относятся к d-семейству. Эти элементы иногда называют переходными металлами. В побочных подгруппах свойства изменяются более медленно, поскольку в атомах d-элементов электроны застраивают второй извне энергетический уровень, а на внешнем уровне находятся только один или два электрона.
Положение первых пяти d-элементов (подгруппы IIIБ- VIIБ) каждого периода можно определить с помощью суммы внешних s-электронов и d-электронов второго снаружи уровня. Например, из электронной формулы скандия (Sc — 4s2 3d1 ) видно, что он размещается в побочной подгруппе (поскольку является d-элементом) третьей группы (поскольку сумма валентных электронов равна трем), а марганец (Mn — 4s2 3d5 ) размещается в побочной подгруппе седьмой группы.
Положение последних двух элементов каждого периода (подгруппы IБ и IIБ) можно определить по количеству электронов на внешнем уровне, поскольку в атомах этих элементов предыдущий уровень является полностью завершенным. Например, Ag ( 5s1 5d10 ) размещается в побочной подгруппе первой группы, Zn ( 4s2 3d10 ) — в побочной подгруппе второй группы.
Триады Fe-Co-Ni, Ru-Rh-Pd и Os-Ir-Pt размещены в побочной подгруппе восьмой группы. Эти триады образуют две семьи: железа и платиноидов. Кроме указанных семей отдельно выделяют семью лантаноидов (четырнадцать 4f-элементов) и семью актиноидов (четырнадцать 5f-элементов). Эти семьи принадлежат к побочной подгруппе третьей группы.
Рост металлических свойств элементов в подгруппах сверху вниз, а также уменьшение этих свойств в пределах одного периода слева направо обусловливают появление в периодической системе диагональной закономерности. Так, Be очень похож на Al, B — на Si, Ti — на Nb. Это ярко проявляется в том, что в природе эти элементы образуют подобные минералы. Например, в природе Те всегда бывает с Nb, образуя минералы — титанониобаты.
www.polnaja-jenciklopedija.ru
Структура периодической системы
Периодическая система химических элементов — это классификация химических элементов, основанная на определенных особенностях строения атомов химических элементов. Она была составлена на основе Периодического закона, открытого в 1869 году Д. И. Менделеевым. В то время Периодическая система включала 63 химических элементов и по виду отличалась от современной. Сейчас в Периодической системы входят около ста двадцати химических элементов.
Периодическую систему составлен в виде таблицы, в которой химические элементы расположены в определенном порядке: по мере роста их атомных масс. Сейчас существует много видов изображения Периодической системы. Наиболее распространенным является изображение в виде таблицы с расположением элементов слева направо.
Все химические элементы в Периодической системе объединены в периоды и группы. Периодическая система включает семь периодов и восемь групп. Периодами называют горизонтальные ряды химических элементов, в которых свойства элементов изменяются от типичных металлических к неметаллическим. Вертикальные колонки химических элементов, которые содержат элементы, схожие по химическим свойствам, образуют группы химических элементов.
Первый, второй и третий периоды называют малыми, поскольку они содержат небольшое количество элементов (первый — два элемента, второй и третий — по восемь элементов). Элементы второго и третьего периодов называют типовыми, их свойства закономерно изменяются от типичного металла до инертного газа.
Все остальные периоды называют большими (четвертый и пятый содержат по 18 элементов, шестой — 32 и седьмой — 24 элемента). Особое сходство свойств проявляют элементы, находящиеся внутри больших периодов, в конце каждого четного ряда. Это так называемые триады: Ферум — Кобальт — Никол, образующих семью железа, и две другие: Рутений — Родий — Палладий и Осмий — Иридий — Платина, которые образуют семью платиновых металлов (платиноидов).
В нижней части таблицы Д. И. Менделеева расположены химические элементы, образующие семью лантаноидов и семью актиноидов. Все эти элементы формально входят в состав третьей группы и идут после химических элементов лантана (номер 57) и актиния (номер 89).
Периодическая система элементов содержит десять рядов. Малые периоды (первый, второй и третий) состоят из одного ряда, большие периоды (четвертый, пятый и шестой) содержат по два ряда каждый. В седьмом периоде находится один ряд.
Каждый большой период состоит из четного и нечетного рядов. В парных рядах содержатся элементы металлы, в нечетных рядах свойства элементов изменяются так, как в типовых элементов, т.е. от металлических до выраженных неметаллических.
Каждая группа таблицы Д. И. Менделеева состоит из двух подгрупп: главной и побочной. В состав главных подгрупп входят элементы как малых, так и больших периодов, то есть главные подгруппы начинаются либо с первого, или второго периода. В состав побочных подгрупп входят элементы только больших периодов, т.е. побочные подгруппы начинаются лишь с четвертого периода.
xn—-7sbfhivhrke5c.xn--p1ai
Периодический закон и периодическая система Менделеева
Периодический закон
Д.И. Менделеев сформулировал Периодический закон в 1869 году, в основе которого была одна из главнейших характеристик атома – атомная масса. Последующее развитие Периодического закона, а именно, получение большого экспериментальных данных, несколько изменило первоначальную формулировку закона, однако эти изменения не противоречат главному смыслу, заложенному Д.И. Менделеевым. Эти изменения только придали закону и Периодической системе научную обоснованность и подтверждение правильности.
Современная формулировка Периодического закона Д.И. Менделеева такова: свойства химических элементов, а также свойства и формы соединений элементов находятся в периодической зависимости от величины заряда ядер их атомов.
Структура Периодической системы химических элементов Д.И. Менделеева
К настоящему мнению известно большое количество интерпретаций Периодической системы, но наиболее популярная – с короткими (малыми) и длинными (большими) периодами. Горизонтальные ряды называют периодами (в них расположены элементы с последовательным заполнением одинакового энергетического уровня), а вертикальные столбцы – группами (в них расположены элементы, имеющие одинаковое количество валентных электронов – химические аналоги). Так же все элементы можно разделить на блоки по по типу внешней (валентной) орбитали: s-, p-, d-, f-элементы.
Всего в системе (таблице) 7 периодов, причем номер периода (обозначается арабской цифрой) равен числу электронных слоев в атоме элемента, номеру внешнего (валентного) энергетического уровня, значению главного квантового числа для высшего энергетического уровня. Каждый период (кроме первого) начинается s-элементом — активным щелочным металлом и заканчивается инертным газом, перед которым стоит p-элемент — активный неметалл (галоген). Если продвигаться по периоду слева направо, то с ростом заряда ядер атомов химических элементов малых периодов будет возрастать число электронов на внешнем энергетическом уровне, вследствие чего свойства элементов изменяются – от типично металлических (т.к. в начале периода стоит активный щелочной металл), через амфотерные (элемент проявляет свойства и металлов и неметаллов) до неметаллических (активный неметалл – галоген в конце периода), т.е. металлические свойства постепенно ослабевают и усиливаются неметаллические.
В больших периодах с ростом заряда ядер заполнение электронов происходит сложнее, что объясняет более сложное изменение свойств элементов по сравнению с элементами малых периодов. Так, в четных рядах больших периодов с ростом заряда ядра число электронов на внешнем энергетическом уровне остается постоянным и равным 2 или 1. Поэтому, пока идет заполнение электронами следующего за внешним (второго снаружи) уровня, свойства элементов в четных рядах изменяются медленно. При переходе к нечетным рядам, с ростом величины заряда ядра увеличивается число электронов на внешнем энергетическом уровне (от 1 до 8), свойства элементов изменяются также, как в малых периодах.
Вертикальные столбцы в Периодической системе – группы элементов со сходным электронным строением и являющимися химическими аналогами. Группы обозначают римскими цифрами от I до VIII. Выделяют главные (А) и побочные (B) подгруппы, первые из которых содержат s- и p-элементы, вторые – d – элементы.
Номер А подгруппы показывает число электронов на внешнем энергетическом уровне (число валентных электронов). Для элементов В-подгрупп нет прямой связи между номером группы и числом электронов на внешнем энергетическом уровне. В А-подгруппах металлические свойства элементов усиливаются, а неметаллические – уменьшаются с возрастанием заряда ядра атома элемента.
Между положением элементов в Периодической системе и строением их атомов существует взаимосвязь:
— атомы всех элементов одного периода имеют равное число энергетических уровней, частично или полностью заполненных электронами;
— атомы всех элементов А подгрупп имею равное число электронов на внешнем энергетическом уровне.
Периодические свойства элементов
Близость физико-химических и химических свойств атомов обусловлена сходством их электронных конфигураций, причем, главную роль играет распределение электронов по внешней атомной орбитали. Это проявляется в периодическом появлении, по мере увеличения заряда ядра атома, элементов с близкими свойствами. Такие свойства называют периодическими, среди которых наиболее важными являются:
1. Количество электронов на внешней электронной оболочке (заселенность – w). В малых периодах с ростом заряда ядра w внешней электронной оболочки монотонно увеличивается от 1 до 2 (1 период), от 1 до 8 (2-й и 3-й периоды). В больших периодах на протяжении первых 12 элементов w не превышает 2, а затем монотонно увеличивается до 8.
2. Атомный и ионный радиусы (r), определяемые как средние радиусы атома или иона, находимые из экспериментальных данных по межатомным расстояниям в разных соединениях. По периоду атомный радиус уменьшается (постепенно прибавляющиеся электроны описываются орбиталями с почти равными характеристиками, по группе атомный радиус возрастает, поскольку увеличивается число электронных слоев (рис.1.).
Рис. 1. Периодическое изменение атомного радиуса
Такие же закономерности наблюдаются и для ионного радиуса. Следует заметить, что ионный радиус катиона (положительно заряженный ион) больше атомного радиуса, а тот в свою очередь, больше ионного радиуса аниона (отрицательно заряженный ион).
3. Энергия ионизации (Еи) – количество энергии, необходимое для отрыва электрона от атома, т.е. энергия, необходимая для превращения нейтрального атома в положительно заряженный ион (катион).
Э0 — → Э+ + Еи
Еи измеряется в электронвольтах (эВ) на атом. В пределах группы Периодической системы значения энергии ионизации атомов уменьшаются с возрастанием зарядов ядер атомов элементов. От атомов химических элементов можно последовательно отрывать все электроны, сообщив дискретные значения Еи. При этом Еи1 < Еи2 < Еи3 <….Энергии ионизации отражают дискретность структуры электронных слоев и оболочек атомов химических элементов.
4. Сродство к электрону (Ее) – количество энергии, выделяющееся при присоединении дополнительного электрона к атому, т.е. энергия процесса
Э0 + → Э—
Ее также выражается в эВ и, как и Еи зависит от радиуса атома, поэтому характер изменения Ее по периодам и группам Периодической системы близок характеру изменения атомного радиуса. Наибольшим сродством к электрону обладают p-элементы VII группы.
5. Восстановительная активность (ВА) – способность атома отдавать электрон другому атому. Количественная мера – Еи. Если Еи увеличивается, то ВА уменьшается и наоборот.
6. Окислительная активность (ОА) – способность атома присоединять электрон от другого атома. Количественная мера Ее. Если Ее увеличивается, то ОА также увеличивается и наоборот.
7. Эффект экранирования – уменьшение воздействия на данный электрон положительного заряда ядра из-за наличия между ним и ядром других электронов. Экранирование растет с увеличением числа электронных слоев в атоме и уменьшает притяжение внешних электронов к ядру. Экранированию противоположен эффект проникновения, обусловленный тем, что электрон может находиться в любой точке атомного пространства. Эффект проникновения увеличивает прочность связи электрона с ядром.
8. Степень окисления (окислительное число) – воображаемый заряд атома элемента в соединении, который определяется из предположения ионного строения вещества. Номер группы Периодической системы указывает высшую положительную степень окисления, которую могут иметь элементы данной группы в своих соединениях. Исключение – металлы подгруппы меди, кислород, фтор, бром, металлы семейства железа и другие элементы VIII группы. С ростом заряда ядра в периоде максимальная положительная степень окисления растет.
9. Электроотрицательность, составы высших водородных и кислородных соединений, термодинамические, электролитические свойства и т.д.
Примеры решения задач
ru.solverbook.com
Периодическая система Менделеева и периодический закон
В период девятнадцатого века сильную реформацию претерпели многие направления, в том числе и химия. Периодическая система Менделеева, сформулированная в 1869 году, привела к единому пониманию зависимости положения простых веществ в таблице Менделеева, установившей взаимосвязь между относительной атомной массой, валентностью и свойством элемента.
Доменделеевский период химии
Несколько ранее, в начале девятнадцатого века, предпринимались неоднократные попытки систематизации химических элементов. Немецкий химик Дёберейнер провёл первую серьёзную работу по систематизации в области химии. Он определил, что ряд сходных веществ по свойствам можно объединить в группы – триады.
Ошибочность представлений немецкого учёного
Суть представленного закона триад Дёберейнера определялась тем, что атомная масса искомого вещества близка к полусумме (среднему значению) атомных масс двух последних элементов таблицы триады.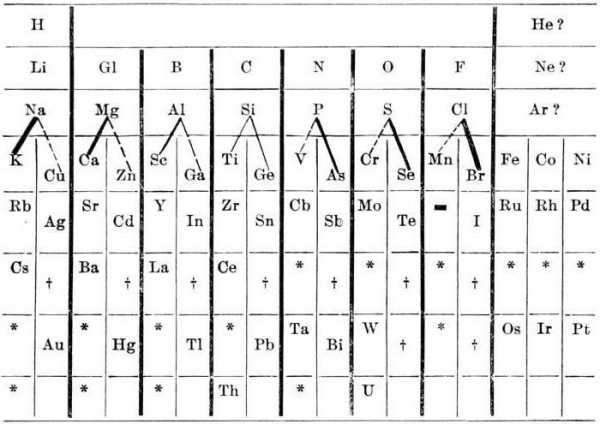 Однако отсутствие магния в единой подгруппе кальция, стронция и бария было ошибочным.
Однако отсутствие магния в единой подгруппе кальция, стронция и бария было ошибочным.
Данный подход являлся следствием искусственного ограничения аналогичных веществ только тройственными союзами. Дёберейнер хорошо видел сходство в химических параметрах фосфора и мышьяка, висмута и сурьмы. Однако он ограничил себя отыскиванием триад. В итоге он не смог прийти к правильной классификации химических элементов.
Разделить существующие элементы на триады Дёберейнеру, безусловно, не удалось, закон явно указывал на присутствие взаимосвязи между относительной атомной массой и свойствами химических простых веществ.
Процесс систематизации химических элементов
Все последующие попытки систематизации опирались на распределение элементов в зависимости от их атомной массы. В дальнейшем гипотеза Дёберейнера была использована другими химиками. Появилось формирование триад, тетрад и пентад (объединение в группы по три, четыре и пять элементов).
Во второй половине девятнадцатого века появилось одновременно несколько работ, основываясь на которых Дмитрий Иванович Менделеев привёл химию к полноценной систематизации химических элементов. Иное строение периодической системы Менделеева привело к революционному пониманию и очевидности механизма распределения простых веществ.
Периодическая система элементов Менделеева
На заседании русского химического сообщества весной 1869 года было зачитано уведомление русского учёного Д. И. Менделеева об открытии им периодического закона химических элементов. В конце этого же года было опубликована первая работа «Основы химии», в нее была включена первая периодическая система элементов.
В конце этого же года было опубликована первая работа «Основы химии», в нее была включена первая периодическая система элементов.
В ноябре 1870 года он показал коллегам дополнение «Естественная система элементов и использование её к указанию качеств неоткрытых элементов». В этом труде Д. И. Менделеев впервые использовал термин «периодический закон». Система элементов Менделеева на основании периодического закона определяла возможность существования не открытых простых веществ и чётко указывала на их свойства.
Исправления и уточнения
В итоге к 1971 году периодический закон и периодическая система элементов Менделеева были доработаны и дополнены русским химиком.
В окончательной статье «Периодическая законность химических элементов» ученый установил определение периодического закона, где указывается, что характеристики простых тел, свойства соединений, а также образуемых ими сложных тел определяются прямой зависимостью согласно их атомному весу.
Несколько позже, в 1872 году, строение периодической системы Менделеева было реорганизовано в классический вид (короткопериодный способ распределения).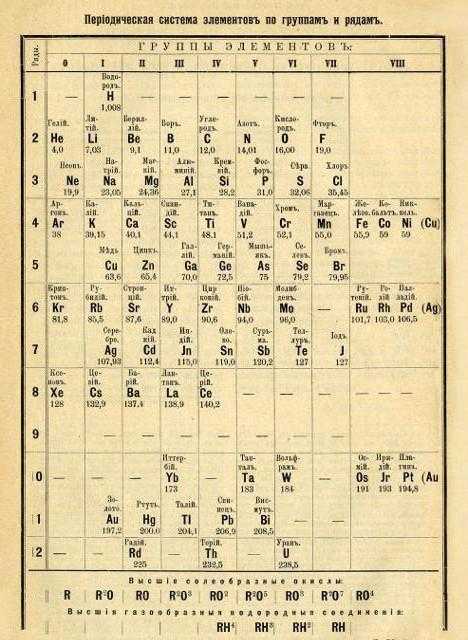
В отличие от предшественников, русский химик полноценно составил таблицу, ввёл понятие закономерности атомного веса химических элементов.
Характеристика элементов периодической системы Менделеева и выведенные закономерности позволили учёному описать свойства элементов, которые еще не открыты. Менделеев опирался на то, что свойства каждого вещества можно определить согласно характеристикам двух соседних элементов. Он назвал это правилом «звезды». Его суть в том, что в таблице химических элементов для определения свойства выбранного элемента необходимо ориентироваться по горизонтали и вертикали в таблице химических элементов.
Периодическая система Менделеева способна предсказать…
Таблица элементов Менделеева, несмотря на свою точность и верность, не была признана научным обществом полноценно. Некоторые великие учёные с мировым именем открыто высмеивали возможность предсказать свойства неоткрытого элемента. И только в 1885 году, после открытия предсказанных элементов – экаалюминия, экабора и экасилиция (галлий, скандий и германий), новая классификационная система Менделеева и периодический закон были признаны в качестве теоретической основы химии.
В начале двадцатого века строение периодической системы Менделеева неоднократно корректировалось. В процессе получения новых научных данных Д. И. Менделеев и его коллега У. Рамзай пришли к заключению о необходимости введения нулевой группы. В её состав вошли инертные газы (гелий, неон, аргон, криптон, ксенон и радон).
В тысяча девятьсот одиннадцатом году Ф. Содди внёс предложение размещать неразличимые химические элементы – изотопы – в одной ячейке таблицы.
В процессе долгой и кропотливой работы таблица периодической системы химических элементов Менделеева была окончательно доработана и приобрела современный вид. В её состав вошло восемь групп и семь периодов. Группы – это вертикальные столбцы, периоды – горизонтальные. В группах определено деление на подгруппы.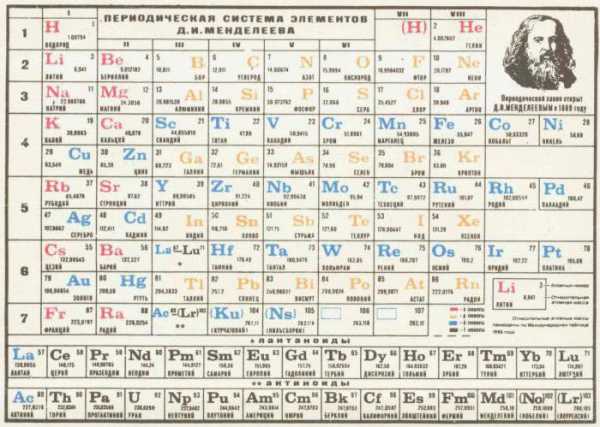
Положение элемента в таблице указывает на его валентность, чисто электронов и химические особенности. Как выяснилось позже, в ходе разработки таблицы Д. И. Менделеевым было обнаружено случайное совпадение количества электронов элемента с его порядковым номером. Этот факт в дальнейшем упростил понимание принципа взаимодействия простых веществ и образование сложных. А также процесс в обратном направлении. Расчёт количества полученного вещества, а также необходимого для протекания химической реакции стал теоретически доступен.
Этот факт в дальнейшем упростил понимание принципа взаимодействия простых веществ и образование сложных. А также процесс в обратном направлении. Расчёт количества полученного вещества, а также необходимого для протекания химической реакции стал теоретически доступен.
Роль открытия Менделеева в современной науке
Система Менделеева и его подход к упорядочиванию химических элементов предопределили дельнейшее развитие химии. Благодаря правильному пониманию взаимосвязи химических констант и анализу Менделеев смог верно скомпоновать и сгруппировать элементы согласно их свойствам. Новая таблица элементов даёт возможность ясно и чётко рассчитывать данные до начала проведения химической реакции, предсказывать новые элементы и их свойства.
Новая таблица элементов даёт возможность ясно и чётко рассчитывать данные до начала проведения химической реакции, предсказывать новые элементы и их свойства.
Открытие русского учёного оказало прямое влияние на дальнейший ход развития науки и технологий. Не существует технологической области, которая бы не задействовала знания химии. Возможно, если бы подобное открытие не состоялось, то наша цивилизация пошла бы по иному пути развития.
fb.ru
ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ | Энциклопедия Кругосвет
Содержание статьиПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ представляет собой классификацию химических элементов в соответствии с периодическим законом, устанавливающим периодическое изменение свойств химических элементов по мере увеличения их атомной массы, связанного с увеличением заряда ядра их атомов; поэтому заряд ядра атома совпадает с порядковым номером элемента в периодической системе и называется атомным номером элемента. Периодическая система элементов оформляется в виде таблицы (периодическая таблица элементов), в горизонтальных рядах которой – периодах – происходит постепенное изменение свойств элементов, а при переходе от одного периода к другому – периодическое повторение общих свойств; вертикальные столбцы – группы – объединяют элементы со сходными свойствами. Периодическая система позволяет без специальных исследований узнать о свойствах элемента только на основании известных свойств соседних по группе или периоду элементов. Физические и химические свойства (агрегатное состояние, твердость, цвет, валентность, ионизация, стабильность, металличность или неметалличность и т.д.) можно предсказывать для элемента на основании периодической таблицы.
В конце 18 и начале 19 вв. химики пытались создавать классификации химических элементов в соответствии с их физическими и химическими свойствами, в частности на основе агрегатного состояния элемента, удельного веса (плотности), электропроводности, металличности – неметалличности, основности – кислотности и т.д.
Классификации по «атомному весу»
(т.е. по относительной атомной массе).
Гипотеза Праута.
В 1805 Дж.Дальтон определил атомные веса нескольких элементов, приняв за единицу атомную массу водорода, а Й.Берцелиус в 1815 значительно уточнил величины атомных весов. Ученые пытались установить простые (целочисленные) соотношения между атомными весами элементов. У.Праут в 1815 предположил, что атомные веса всех элементов связаны простыми кратными отношениями с атомным весом водорода. Но более точные определения атомных весов, выполненные Ж.Дюма и особенно Берцелиусом, а впоследствии и Ж.Стасом, разрушили гипотезу Праута, так как были получены дробные величины атомных весов. И только в начале 20 в., когда стало известно строение атома, идеи Праута возродились.
Триады Доберейнера.
И.Доберейнер в 1816–1829 установил, что для триад сходных элементов, таких, как Cl, Br, I и Ca, Sr, Ba, атомные массы и величины некоторых физических свойств находятся в арифметической прогрессии и для каждого второго элемента свойство можно предсказать как среднее между свойствами двух крайних. Существование такой прямой взаимосвязи для всех элементов казалось вероятным, но количественная оценка была невозможна из-за путаницы между атомными и эквивалентными весами до тех пор, пока С.Канниццаро в 1858 не пересмотрел величины атомных весов.
Октавы Ньюлендса.
Дж.Ньюлендс в 1864, анализируя все известные триады и расширяя по возможности их в семейства по 4–5 элементов, получил общую таблицу, что позволило ему предположить существование одного или двух неоткрытых элементов. Затем он перестроил классификацию элементов в порядке увеличения атомного веса и обнаружил периодическую повторяемость свойств у каждого восьмого элемента. К сожалению, Ньюлендс не оставил свободные места в таблице для неоткрытых элементов, а его предложение назвать новую таблицу законом октав встретило холодный прием.
Периодический закон.
Два других химика, русский ученый Д.И.Менделеев и немецкий ученый Л.Мейер независимо друг от друга предложили классификацию элементов в виде семейств, в которых периодически повторяются сходные свойства, когда элементы расположены в порядке увеличения атомного веса. Оба опубликовали свои таблицы (Менделеев – в 1869, а Мейер – в 1870) и дали формулировку нового открытого периодического закона. Уверенность Менделеева в правильности периодического закона была так велика, что он не колеблясь исправил известные значения атомных весов на основании открытого закона. Он предсказал существование и довольно точно описал свойства трех новых, еще неизвестных тогда элементов, которые были открыты через несколько лет: галлия (1875), скандия (1879) и германия (1886).
Периодическая таблица.
Менделеев расположил элементы в порядке увеличения их атомного веса и в 1869 предложил таблицу размещения семейств элементов (табл. 1). Модифицированная форма таблицы (табл. 2), в которой семейства (группы) элементов расположены в колонках, была предложена им в 1871 и существует до настоящего времени. Наряду с ней получила распространение развернутая форма таблицы. См. также ХИМИЯ; ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ.
| Таблица 1. ПЕРИОДИЧЕСКАЯ ТАБЛИЦА ЭЛЕМЕНТОВ, ОПУБЛИКОВАННАЯ МЕНДЕЛЕЕВЫМ В 1869 (первая версия) | |||||
| Ti = 50 | Zr = 90 | ? = 180 | |||
| V = 51 | Nb = 94 | Ta = 182 | |||
| Cr = 52 | Mo = 96 | W = 186 | |||
| Mn = 55 | Rh = 104,4 | Pt = 197,4 | |||
| Fe = 56 | Ru = 104,4 | Ir = 198 | |||
| Ni = | Co = 59 | Pd = 106,6 | Os = 199 | ||
| H = 1 | Cu = 63,4 | Ag = 108 | Hg = 200 | ||
| Be = 9,4 | Mg = 24 | Zn = 65,2 | Cd = 112 | ||
| B = 11 | Al = 27,4 | ? = 68 | Ur = 116 | Au = 197? | |
| C = 12 | Si = 28 | ? = 70 | Sn = 118 | ||
| N = 14 | P = 31 | As = 75 | Sb = 122 | Bi = 210? | |
| O = 16 | S = 32 | Se = 79,4 | Te = 128? | ||
| F = 19 | Cl = 35,5 | Br = 80 | I = 127 | ||
| Li = 7 | Na = 23 | K = 39 | Rb = 85,4 | Cs = 133 | Tl = 204 |
| Ca = 40 | Sr = 87,6 | Ba = 137 | Pb = 207 | ||
| ? = 45 | Ce = 92 | ||||
| ?Er = 56 | La = 94 | ||||
| ?Yt = 60 | Di = 95 | ||||
| ?In = 75,6 | Th = 118 | ||||
| Таблица 2. МОДИФИЦИРОВАННАЯ ТАБЛИЦА МЕНДЕЛЕЕВА | |||||||||||||||||||||||||
| Группа | I | II | III | IV | V | VI | VII | VIII | 0 | ||||||||||||||||
| Формула оксида или гидрида Подгруппа | R2O А В | RO А В | R2O3 В А | RH4 RO2 В А | RH3 R2O5 В А | RH2 RO3 В А | RH R2O7 В А | ||||||||||||||||||
| Период 1 | 1 H Водород 1,0079 | 2 He Гелий 4,0026 | |||||||||||||||||||||||
| Период 2 | 3 Li Литий 6,941 | 4 Be Бериллий 9,0122 | 5 B Бор 10,81 | 6 C Углерод 12,011 | 7 N Азот 14,0067 | 8 O Кислород 15,9994 | 9 F Фтор 18,9984 | 10 Ne Неон 20,179 | |||||||||||||||||
| Период 3 | 11 Na Натрий 22,9898 | 12 Mg Магний 24,305 | 13 Al Алюминий 26,9815 | 14 Si Кремний 28,0855 | 15 P Фосфор 30,9738 | 16 S Сера 32,06 | 17 Cl Хлор 35,453 | 18 Ar Аргон 39,948 | |||||||||||||||||
| Период 4 | 19 K Калий 39,0983 29 Cu Медь 63,546 | 20 Ca Кальций 40,08 30 Zn Цинк 65,39 | 21 Sc Скандий 44,9559 31 Ga Галлий 69,72 | 22 Ti Титан 47,88 32 Ge Германий 72,59 | 23 V Ванадий 50,9415 33 As Мышьяк 74,9216 | 24 Cr Хром 51,996 34 Se Селен 78,96 | 25 Mn Марганец 54,9380 35 Br Бром 79,904 | 26 Fe Железо 55,847 | 27 Co Кобальт 58,9332 | 28 Ni Никель 58,69 | 36 | ||||||||||||||
| Период 5 | 37 Rb Рубидий 85,4678 47 Ag Серебро 107,868 | 38 Sr Стронций 87,62 48 Cd Кадмий 112,41 | 39 Y Иттрий 88,9059 49 In Индий 114,82 | 40 Zr Цирконий 91,22 50 Sn Олово 118,69 | 41 Nb Ниобий 92,9064 51 Sb Сурьма 121,75 | 42 Mo Молибден 95,94 52 Te Теллур 127,60 | 43 Tc Технеций [97] 53 I Иод 126,9044 | 44 Ru Рутений 101,07 | 45 Rh Родий 102,9055 | 46 Pd Палладий 106,4 | 54 | ||||||||||||||
| Период 6 | 55 Cs Цезий 132,9054 79 Au Золото 196,9665 | 56 Ba Барий 137,33 80 Hg Ртуть 200,59 | 57* La Лантан 138,9055 81 Tl Таллий 204,38 | 72 Hf Гафний 178,49 82 Pb Свинец 207,21 | 73 Ta Тантал 180,9479 83 Bi Висмут 208,9804 | 74 W Вольфрам 183,85 84 Po Полоний [209] | 75 Re Рений 186,207 85 At Астат [210] | 76 Os Осмий 190,2 | 77 Ir Иридий 192,2 | 78 Pt Платина 195,08 | 86 | ||||||||||||||
| Период 7 | 87 Fr Франций [223] | 88 Ra Радий 226,0254 | 89** Ac Актиний 227,028 | 104 [261] | 105 [258] | 106 [260] | 107 [262] | 108 [265] | 109 [266] |
| |||||||||||||||
| * | 58 Ce 140,12 | 59 Pr 140,9077 | 60 Nd 144,24 | 61 Pm [145] | 62 Sm 150,36 | 63 Eu 151,96 | 64 Gd 157,25 | 65 Tb 158,9254 | 66 Dy 162,50 | 67 Ho 164,9304 | 68 Er 167,26 | 69 Tm 168,9342 | 70 Yb 173,04 | 71 Lu 174,967 | |||||||||||
| ** | 90 Th 232,0381 | 91 Pa 231,0359 | 92 U 238,0289 | 93 Np 237,0482 | 94 Pu [244] | 95 Am [243] | 96 Cm [247] | 97 Bk [247] | 98 Cf [251] | 99 Es [252] | 100 Fm [257] | 101 Md [258] | 102 No [259] | 103 Lr [260] | |||||||||||
| *Лантаноиды: церий, празеодим, неодим, прометий, самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий, иттербий, лютеций. **Актиноиды: торий, протактиний, уран, нептуний, плутоний, америций, кюрий, берклий, калифорний, эйнштейний, фермий, менделевий, нобелий, лоуренсий. Примечание. Атомный номер указан над символом элемента, атомная масса указана под символом элемента. Величина в скобках – массовое число наиболее долгоживущего изотопа. | |||||||||||||||||||||||||
Периоды.
В этой таблице Менделеев расположил элементы в горизонтальных рядах – периодах. Таблица начинается с очень короткого периода, содержащего только водород и гелий. Следующие два коротких периода содержат по 8 элементов. Затем располагаются четыре длинных периода. Все периоды, кроме первого, начинаются со щелочного металла (Li, Na, K, Rb, Cs), и все периоды заканчиваются благородным газом. В 6-м периоде находится серия из 14 элементов – лантаноиды, которой формально нет места в таблице и ее обычно располагают под таблицей. Другая аналогичная серия – актиноиды – находится в 7-м периоде. Эта серия включает элементы, полученные в лаборатории, например бомбардировкой урана субатомными частицами, и также размещается под таблицей ниже лантаноидов.
Группы и подгруппы.
При расположении периодов друг под другом элементы располагаются в колонки, образуя группы, нумеруемые цифрами 0, I, II,…, VIII. Предполагается, что элементы внутри каждой группы проявляют сходные общие химические свойства. Еще бóльшее сходство наблюдается у элементов в подгруппах (A и B), которые образуются из элементов всех групп, кроме 0 и VIII. Подгруппа А называется главной, а В – побочной. Некоторые семейства имеют названия, например, щелочные металлы (группа IA), щелочноземельные металлы (группа IIA), галогены (группа VIIA) и благородные газы (группа 0). В группе VIII находятся переходные металлы: Fe, Co и Ni; Ru, Rh и Pd; Os, Ir и Pt. Находящиеся в середине длинных периодов, эти элементы более сходны друг с другом, чем с элементами, стоящими до и после них. В нескольких случаях порядок увеличения атомных весов (точнее, атомных масс) нарушается, например, в пáрах теллур и иод, аргон и калий. Это «нарушение» необходимо для сохранения сходства элементов в подгруппах.
Металлы, неметаллы.
Диагональ от водорода к радону примерно делит все элементы на металлы и неметаллы, при этом неметаллы находятся выше диагонали. (К неметаллам относят 22 элемента – H, B, C, Si, N, P, As, O, S, Se, Te, галогены и инертные газы, к металлам – все остальные элементы.) Вдоль этой линии располагаются элементы, которые обладают некоторыми свойствами металлов и неметаллов (металлоиды – устаревшее название таких элементов). При рассмотрении свойств по подгруппам сверху вниз наблюдается увеличение металлических свойств и ослабление неметаллических свойств.
Валентность.
Наиболее общее определение валентности элемента – это способность его атомов соединяться с другими атомами в определенных соотношениях. Иногда валентность элемента заменяют близким ему понятием степени окисления (с.о.). Степень окисления соответствует заряду, который приобрел бы атом, если бы все электронные пары его химических связей сместились в сторону более электроотрицательных атомов. В любом периоде слева направо происходит увеличение положительной степени окисления элементов. Элементы I группы имеют с.о., равную +1 и формулу оксида R2O, элементы II группы – соответственно +2 и RO и т.д. Элементы с отрицательной с.о. находятся в V, VI и VII группах; считается, что углерод и кремний, находящиеся в IV группе, не имеют отрицательной степени окисления. Галогены, имеющие степень окисления –1, образуют соединения с водородом состава RH. В целом положительная степень окисления элементов соответствует номеру группы, а отрицательная равна разности восемь минус номер группы. Из таблицы нельзя определить наличие или отсутствие других степеней окисления.
Физический смысл атомного номера.
Истинное понимание периодической таблицы возможно только на основе современных представлений о строении атома. Порядковый номер элемента в периодической таблице – его атомный номер – значительно важнее величины его атомного веса (т.е. относительной атомной массы) для понимания химических свойств.
Строение атома.
В 1913 Н.Бор использовал ядерную модель строения атома для объяснения спектра атома водорода, наиболее легкого и поэтому наиболее простого атома. Бор предположил, что атом водорода состоит из одного протона, составляющего ядро атома, и одного электрона, вращающегося вокруг ядра.
Определение понятия атомного номера.
В 1913 А.ван ден Брук предположил, что порядковый номер элемента – его атомный номер – должен идентифицироваться с числом электронов, вращающихся вокруг ядра нейтрального атома, и с положительным зарядом ядра атома в единицах заряда электрона. Однако необходимо было экспериментальное подтверждение идентичности заряда атома и атомного номера. Бор далее постулировал, что характеристическое рентгеновское излучение элемента должно подчиняться такому же закону, что и спектр водорода. Так, если атомный номер Z идентифицируется с зарядом ядра в единицах заряда электрона, то частоты (длины волн) соответствующих линий в рентгеновских спектрах различных элементов должны быть пропорциональны Z2, квадрату атомного номера элемента.
В 1913–1914 Г.Мозли, изучая характеристическое рентгеновское излучение атомов различных элементов, получил блестящее подтверждение гипотезы Бора. Работа Мозли таким образом подтвердила предположение ван ден Брука об идентичности атомного номера элемента с зарядом его ядра; атомный номер, а не атомная масса, является истинной основой для определения химических свойств элемента.
Периодичность и атомная структура.
Квантовая теория Бора строения атома развивалась в течение двух десятилетий после 1913. Предложенное Бором «квантовое число» стало одним из четырех квантовых чисел, необходимых для характеристики энергетического состояния электрона. В 1925 В.Паули сформулировал свой знаменитый «принцип запрета» (принцип Паули), согласно которому в атоме не может быть двух электронов, у которых бы все квантовые числа были одинаковые. Когда этот принцип применили к электронным конфигурациям атомов, периодическая таблица приобрела физическое обоснование. Так как атомный номер Z, т.е. положительный заряд ядра атома, возрастает, то и количество электронов должно возрастать для сохранения электронейтральности атома. Эти электроны определяют химическое «поведение» атома. Согласно принципу Паули, по мере увеличения значения квантового числа электроны заполняют электронные слои (оболочки) начиная с ближайших к ядру. Завершенный слой, который заполнен всеми электронами в соответствии с принципом Паули, является наиболее стабильным. Поэтому благородные газы, такие, как гелий и аргон, имеющие полностью завершенные электронные структуры, устойчивы к любому химическому воздействию.
Электронные конфигурации.
В следующей таблице приведены возможные количества электронов для различных энергетических состояний. Главное квантовое число n = 1, 2, 3,… характеризует энергетический уровень электронов (1-й уровень располагается ближе к ядру). Орбитальное квантовое число l = 0, 1, 2,…, n – 1 характеризует орбитальный момент импульса. Орбитальное квантовое число всегда меньше главного квантового числа, а максимальное его значение равно главному минус 1. Каждому значению l отвечает определенный тип орбитали – s, p, d, f … (это обозначение происходит от спектроскопической номенклатуры 18 в., когда различные серии наблюдаемых спектральных линий назывались sharp, principal, diffuse и fundamental).
| Таблица 3. ЧИСЛО ЭЛЕКТРОНОВ В РАЗЛИЧНЫХ ЭНЕРГЕТИЧЕСКИХ СОСТОЯНИЯХ АТОМА | |||
| Главное квантовое число | Орбитальное квантовое число | Количество электронов на оболочке | Обозначение энергетического состояния (тип орбитали) |
| 1 | 0 | 2 | 1s |
| 2 | 0 | 2 | 2s |
| 1 | 6 | 2p | |
| 3 | 0 | 2 | 3s |
| 1 | 6 | 3p | |
| 2 | 10 | 3d | |
| 4 | 0 | 2 | 4s |
| 1 | 6 | 4p | |
| 2 | 10 | 4d | |
| 3 | 14 | 4f | |
| 5 | 0 | 2 | 5s |
| 1 | 6 | 5p | |
| 2 | 10 | 5d | |
| 5 | 14 | 5f | |
| 4 | 18 | 5g | |
| 6 | 0 | 2 | 6s |
| 1 | 6 | 6p | |
| 2 | 10 | 6d | |
| … | … | … | … |
| 7 | 0 | 2 | 7s |
Короткие и длинные периоды.
Низшая полностью завершенная электронная оболочка (орбиталь) обозначается 1s и реализуется у гелия. Следующие уровни – 2s и 2p – соответствуют застройке оболочек атомов элементов 2-го периода и при полной застройке, у неона, содержат в сумме 8 электронов. С увеличением значений главного квантового числа энергетическое состояние низшего орбитального числа для большего главного может оказаться ниже энергетического состояния наиболее высокого орбитального квантового числа, соответствующего меньшему главному. Так, энергетическое состояние 3d выше, чем 4s, поэтому у элементов 3-го периода происходит застройка 3s– и 3p-орбиталей, заканчиваясь формированием устойчивой структуры благородного газа аргона. Далее происходит последовательная застройка 4s-, 3d– и 4p-орбиталей у элементов 4-го периода, вплоть до завершения внешней устойчивой электронной оболочки из 18 электронов у криптона. Это и приводит к появлению первого длинного периода. Аналогично происходит застройка 5s-, 4d– и 5p-орбиталей атомов элементов 5-го (т.е. второго длинного) периода, завершаясь электронной структурой ксенона.
Лантаноиды и актиноиды.
Последовательное заполнение электронами 6s-, 4f-, 5d– и 6p-орбиталей у элементов 6-го (т.е. третьего длинного) периода приводит к появлению новых 32 электронов, которые формируют структуру последнего элемента этого периода – радона. Начиная с 57 элемента, лантана, последовательно располагаются 14 элементов, мало отличающихся по химическим свойствам. Они образуют серию лантаноидов, или редкоземельных элементов, у которых застраивается 4f-оболочка, содержащая 14 электронов.
Серия актиноидов, которая располагается за актинием (атомный номер 89), характеризуется застройкой 5f-оболочки; она также включает 14 элементов, весьма близких по химическим свойствам. Элемент с атомным номером 104 (резерфордий), следующий за последним из актиноидов, уже отличается по химическим свойствам: он является аналогом гафния. Для элементов за резерфордием приняты названия: 105 – дубний (Db), 106 – сиборгий (Sg), 107 – борий (Bh), 108 – хассий (Hs), 109 – мейтнерий (Mt).
Применение периодической таблицы.
Знание периодической таблицы позволяет химику предсказывать с определенной степенью точности свойства любого элемента, прежде чем он приступит к работе с ним. Металлурги, например, считают периодическую таблицу полезной для создания новых сплавов, так как, используя периодическую таблицу, можно заменить один из металлов сплава, подобрав ему замену среди его соседей по таблице так, что с определенной степенью вероятности не произойдет значительного изменения свойств образующегося из них сплава.
www.krugosvet.ru
Периодическая система Менделеева • Джеймс Трефил, энциклопедия «Двести законов мироздания»
Господин Менделеев не знал, а его последователи узнали, но начисто позабыли или антинаучно проигнорировали то, что атомы есть комплементарные пары из взаимно дополнительных вложенных друг в друга фундаментальных сущностей вещества: ядер атомов как внутренней сущности и электронных облаков как внешней сущности. Иначе говоря, атомы есть фракталы вложенностей – матрёшки.Отсюда следует, что на самом деле натуральный ряд элементов представляет собой не один ряд элементов, а два комплементарных ряда фундаментальных сущностей вещества – ядер атомов и электронных облаков!
Следующий грубейший научный промах Менделеева и его последователей: начало каждого периода щелочным металлом и окончание благородным газом. Ведь в первом периоде Периодической системы элементов в редакции Менделеева до 1902 года первым являлся не щелочной металл, а неметалл химически активный двух атомный газ водород, имеющий крайне низкую температуру кипения! В то время, как во всех последующих периодах первым был элемент группы щёлочноземельных металлов. Прокол в Периодической таблице элементов жутчайший! А в периодической таблице элементов в редакции Менделеева от 1902 и 1906 годов первым элементом в периодах являлся элемент группы благородных газов.
Правильные, естественные окончания абсолютно каждого периода атомного мира материи является не благородный газ, а щёлочноземельный металл – по Мейеру Ю.Л. (приоритет от 1862 года на правильное окончание периодов на элементе группы щёлочноземельных металлов), Менделееву Д.И. (приоритет от 1869 и 1870 годов на правильное предсказание свойств нескольких не известных тогда элементов и исправление атомных масс нескольких известных элементов, а также на формулировку формулы периодического явления, ошибочно названного и до сих пор ошибочно считающегося периодическим законом, и приоритет от 1902 года на гипотезу о двух элементах материального эфира – ньютония и корония, предшествующих водороду), Веберу А. (приоритет от 1905 года на идею отображать каждый из всех периодов одним рядом), Жанету Ч. (приоритет от 1928 года на отображение каждого из всех правильных периодов одним рядом), Резерфорду Э. (приоритет от 1911 года на правильное объяснение устройства атомов из компактного электростатически положительно заряженного ядра и обширного электростатически отрицательного заряженного электронного облака), Мозли Г. (приоритет от 1913 года на экспериментальное, по рентгеновскому спектру, доказательство того, что номер элемента равен количеству протонов я ядре атома или количеству электронов в электронном облаке не ионизированного атома), Бору Н. (приоритет от 1913 года на идею о стационарных орбитах не возбуждённых электронов в оболочках слоёв электронного облака атома), и Макееву А.К. (приоритет от 2000, 2010, 2013 годы на пакет свыше 20 настоящих периодических законов и фундаментальных научных положений, описывающих строение и порядок формирования электронного облака атома по мере роста электростатического заряда ядер атомов; на расширение периодической системы элементов перед водородом на 10 элементов вакуумных уровней материи; создание модели строения материи вакуума и фотона, теоретического доказательства того, что кванты электростатического и магнитного полей в составе материи фотона в их векторах движения имеют скорость в корень квадратный из двух раз быстрее движения всей системы материи фотона в его векторе движения)!
Тогда мировой науке официально следует принять то что первый правильный (естественный) период атомных уровней материи содержит 4 элемента, которые радикально отличаются друг от друга по физическим и химическим свойствам: водород (химический активный двух атомный газ), гелий (химически инертный одно атомный газ), литий (химически активный щелочной металл) и бериллий (химически активный щёлочноземельный металл-металлоид). Поэтому последние 4 элемента каждого последующего правильного (естественного) периода позиционно аналогичны неметаллу химически активному подобному галогенам двухатомному газу водороду, неметаллу химически инертному одноатомному газу гелию, химически активному щелочному металлу литию и химически активному щёлочноземельному металлу бериллию!
В Матрице автоматизма материи – периодической таблице элементов вакуумных и атомных уровней материи Мейера, Жанета и Макеева проявляется очень важный запрет-закон Макеева, не замеченный Паули – запрет каждому слою электронного облака атома заполнять больше чем одну его оболочку в пределах каждого такого естественного периода, в котором этот слой заполняется электронами.
Смотрите подробности здесь:
1. Makeyev A.K. Julius Lothar Meyer was first which built the periodic table of elements // Eropean applied sciences, April, 2013, 4 (2) – pp. 49-61. ISSN 2195-2183
2. Макеев А.К. Система естественных циклов автоматизмов материи. Материалы 1-ой международной научно-практической конференции “Перспективы развития естествознания в 21 веке” // Апробация. Ежемесячный научно-практический журнал, № 2, 2012. 110 с., С. 88-100. ISSN 2305-4484
3. Макеев А.К. Частицы электростатического и магнитного полей в системе материи фотона движутся намного быстрее, чем движется сам фотон. // Научная дискуссия: материалы IV международной заочной научно-практической конференции. Часть I. (20 августа 2012) – Москва: Изд. “Международный центр науки и образования”, 2012. 142 с., С. 47-65. ISBN 978-5-905945-37-3 УДК 08. ББК 94. Н 34. http://www.internauka.org/node/479
4. Макеев А.К. Матрица автоматизмов материи и матрица элементарных артикуляций в каркасе голограммы всезнания // Научно-техническая библиотека. 27 марта 2013. 84 с. http://www.sciteclibrary.ru/rus/catalog/pages/12751.html
Кстати, авторитет и приоритет России, как родины фундаментальной азбучной истины физикохимии – Естественной системы элементов нисколько не пострадал! Ведь автором этой “периодической таблицы” элементов в правильных границах всех периодов и пакета из более чем двадцати настоящих периодических законов и фундаментальных научных положений является гражданин России, москвич Макеев Александр Константинович, врач и мультидисциплинарный исследователь и изобретатель, с приоритетом от 2000 года! В соавторстве с немецким врачом, физиком и химиком Мейером Юлиусом Лотаром, с приоритетом от 1862 года. И в соавторстве с французским инденером и учёным, предпринимателем Жанетом Чарльзом, с приоритетом от 1928 года.
Менделеева по справедливости не наградили Нобелевской Премией в 1906 году. Ведь его Периодическая таблица химических элементов грубо не верна в окончаниях всех периодов! Он даже не смог сформулировать ни одного настоящего периодического закона!
Теперь Комитет по присуждению Премии им. Альфреда Нобеля может с чистой душой, не опасаясь проявления со временем подвоха, присудить свою высокую Премию настоящему создателю Естественной системы элементов и открывателю целого пакета настоящих периодических законов россиянину Макееву Александру Константиновичу! Ау, нынешние Нобелевские Лауреаты, имеющие на то право, замолвите словечко в Нобелевский Комитет, пожалуйста!
elementy.ru