Как сдать экзамен по химии – 7 важных советов, как готовиться к ЕГЭ по химии. Все нужные таблицы, формулы и пособия
- Комментариев к записи Как сдать экзамен по химии – 7 важных советов, как готовиться к ЕГЭ по химии. Все нужные таблицы, формулы и пособия нет
- Советы абитуриенту
- как сдать ЕГЭ по химии — Учёба.ру
- 7 важных советов, как готовиться к ЕГЭ по химии. Все нужные таблицы, формулы и пособия
- 1. Найдите человека, которому вы сможете задавать вопросы
- 2. На экзамене у вас будет три официальные шпаргалки. И в них нужно разбираться
- 3. Повторяйте математику. Химию без неё не сдать
- 4. Таблица химических реакций — ваш помощник
- 5. Берите книжки ФИПИ и идите от простого к сложному
- 6. Теория хорошо, но без тестов всё равно никуда
- 7. А вот читать лишние статьи и литературу точно не нужно
- Готовимся сдавать экзамен по химии – полезные советы
- как успешно сдать экзамен по химии. Рекомендации.
- Как сдать экзамен по химии Как? Так!
- Как сдать ЕГЭ по химии: советы и рекомендации
- Как запомнить термины к экзамену ЕГЭ по химии. Советы!
как сдать ЕГЭ по химии — Учёба.ру

Елена Батаева,
преподаватель химии в школе «Интеллектуал»,
доцент химфака МГУ
В чем, по-вашему, самая большая сложность ЕГЭ по химии? Есть ли в этом году какие-то существенные изменения в структуре экзамена?
В этом году структура экзамена изменилась, в варианте 2017 года не осталось вопросов, которые предполагают выбор только одного ответа. Теперь все задания будут с выбором минимум двух ответов. Принципиально они не сложнее, но так как надо выбирать два раза, вероятность ошибки возрастает. Таким образом, получается, что экзамен стал чуть труднее.
Заданий теперь меньше — осталось 34 задания: пять — в части 2, которая раньше называлась «часть С»: решения этих заданий пишутся от руки, и их проверяет эксперт. И 29 заданий в части 1, той, которую проверяет компьютер. Стоит отметить, что именно в этой части дети делают больше всего ошибок. Почему это происходит, сложно сказать: мы не имеем возможности анализировать часть, которую проверяет машина, и апелляций по части 1 нет.
Скорее всего, существенная доля этих ошибок не зависит от конкретного предмета и связана с невнимательностью или волнением на экзамене. Экзамен по химии очень сложным назвать нельзя, те, кто нормально занимался на профильном уровне, должен, по идее, справиться. Но я смотрела статистику, несколько лет назад были такие цифры — 10-12% сдают предмет неудовлетворительно, то есть не набирают минимум, (а это всего 14 баллов из 60 первичных). Вторичный средний балл тоже очень невысокий — около 50 баллов из 100. Я не очень понимаю, как так получается, и меня это вопрос гложет. Что-то здесь не так.
Какие темы, по вашим наблюдениям, хуже всего даются школьникам? Какие вопросы традиционно считаются самыми сложными?
По моим ощущениям, хуже всего у школьников получается решать задания на проверку эмпирических знаний — свойств конкретных элементов и их соединений, то есть «Химия элементов». Есть задания, для решения которых надо предъявить довольно простое знание, — например, задания № 6 (выбрать вещество, которое реагирует с предложенным в задании), № 8 и № 9 (выбрать формулы веществ, участвующих в цепочке превращений из двух шагов). Есть задание № 11, в котором нужно соотнести вещество и несколько веществ, с которыми оно будет реагировать, — традиционно это задание оказывается одним из самых сложных.
Тяжело даются некоторые задания по органической химии, особенно задания № 18 и № 19, где требуется соотнести реагенты и продукты реакции. Дело в том, что в большинстве случаев продукт однозначен, но иногда бывает, что процесс описан неоднозначно. Ученик выбирает не тот вариант ответа, на который рассчитывал составитель. При этом, вполне возможно, что ход рассуждений был верным, и, если бы это задание проверял эксперт, то он понял бы, что мысль идет в правильном направлении, но при механической проверке просто фиксируется ошибка.
Есть задания № 27, № 28 и № 29, которые, по сути, очень простые, но в них легко ошибиться. Это расчетные задачи, решение которых состоит из нескольких простых шагов. На любом этапе можно сделать ошибку и «протащить» ее дальше. Да еще и в ответе, где указано «запишите число с точностью до …», можно неудачно округлить.
Но самое неприятное для школьника задание, на мой взгляд, — это задание № 26, в которое входят вопросы по производству и области применения. Эти вопросы в школьной программе обсуждаются в разных темах, и не всегда в конце курса удается обобщить и повторить их. Ответ на вопрос этого задания требует не только воспроизвести информацию из различных разделов химии, но и применить общую эрудицию, которой у школьника может не быть. Это вопрос сразу про все: про жизнь, про производство, про применение. Редкий ребенок сможет ответить, для производства какого полимера используется терефталевая кислота, даже если в 10 классе он это знал.
Какие вопросы дают больше всего баллов? На что стоит обратить внимание?
Вся часть 2, которая пишется от руки и проверяется экспертом, в сумме дает 20 баллов. Каждое задание здесь «весит» больше одного балла: за задание № 30 можно получить до 3 баллов, за задание № 31 — максимум 4 балла, за задание № 32 — 5 баллов, а задания № 33 и № 34 дают до 4 баллов.
В задании № 31 в текстовой форме описано проведение эксперимента, и надо описать его в форме уравнений реакций. Это достаточно сложное задание, потому что если школьник не делал или не видел эксперимента, справиться тяжело.
Задание № 32 — органическая цепочка, одно из самых сложных, поскольку школьники тут могут что-то упустить: написать схему вместо уравнения, не написать все продукты и так далее.
Все задания части 2 достаточно сложные, но нужно попытаться их сделать. Даже если не все понятно — решить хотя бы часть задач, «отгрызть» хотя бы часть баллов, потому что там оценка суммируется: написал уравнение — получил 1 балл, посчитал — еще 1 балл, и так далее.
Как лучше готовиться к экзамену по химии?
В апреле к ЕГЭ начинать готовиться, конечно, поздновато. Правильной стратегией было бы все время учить химию, не задумываясь об экзамене, — химия, которую дают в школе на профильном уровне, несколько выше, чем требует ЕГЭ. Если школьник нормально учил этот предмет на профильном уровне, ему достаточно в апреле-мае взять с сайта ФИПИ вопросы, купить книжку с вариантами и по ним потренироваться с этой формой. Если что-то не получается, есть возможность подойти к преподавателю и поинтересоваться, мол, а что я делаю не так.
Любой школьный учебник по химии для профильного уровня подойдет для подготовки. Их несколько, и все профильные учебники приличные. «Профильный» или «углубленный» здесь ключевые слова, поскольку учебники для базового уровня не подходят для подготовки к ЕГЭ, они просто предназначены для другой аудитории.
Не все, конечно, зависит от самого ученика. Дело в том, что химия — это наука о веществе, и, по-хорошему, ее надо начинать со знакомства с веществом, с чувства вещества, чтобы она не стала набором странных и непонятных формул. В некоторых учебниках химия начинается с абстракции, со строения атома. Тогда она и становится набором формул, и это очень тяжело — у ребенка даже в 8 классе, как правило, не сформировано абстрактное мышление, психологически ребенок не готов к оперированию большим числом абстрактных понятий.
Химия — это вообще «про реальное», это экспериментальная наука, без опытов здесь никак, заучивать бесполезно. Официальная программа по химии начинается в 8 классе, но во многих школах за год до этого вводится пропедевтический курс: в течение года дети проводят реакции и опыты, а потом уже узнают про формулы.
Что может сделать школьник, если ему не повезло, и подобного курса не было? Сейчас в интернете выкладывается очень много видеозаписей опытов. Можно хотя бы смотреть, раз не можешь сделать сам. Когда есть привязка к чему-то реальному, все становится гораздо проще. Записи экспериментов имеются на портале «Российское образование», но на этом сайте очень сложно что-либо найти. Есть ресурс «Дети и наука», где в разделе «Химия» опубликованы по некоторым темам конспекты, описан конкретный, реальный эксперимент, и к нему снято видео. В крайнем случае можно все найти на YouTube.
www.ucheba.ru
7 важных советов, как готовиться к ЕГЭ по химии. Все нужные таблицы, формулы и пособия
До ЕГЭ по химии осталось совсем немного — меньше полугода (вот тут календарь ЕГЭ-2018). Но наверстать упущенное и разобраться наконец в таблице растворимости и формулах — не поздно. И не только в них, если составить чёткий план и выбрать правильные материалы. О подготовке к ЕГЭ по химии — преподаватель химии и автор телеграм-канала «ФарСмацевтика» Анна Тихонова.
Рассылка «Мела»
Мы отправляем нашу интересную и очень полезную рассылку два раза в неделю: во вторник и пятницу
В этом году форма экзамена почти не изменилась: вместо 34 заданий их будет 35. Но из-за этого немного изменится система пересчёта первичных баллов в тестовые. Экзамен состоит из двух частей: первая предполагает выбор цифр или последовательности цифр (29 заданий), вторая — ответы с развёрнутым ответом (6 заданий). Максимальное количество первичных баллов, которое можно набрать за первую часть, — 40, за вторую — 20. Обычно мои ученики начинают паниковать уже на этой стадии — когда узнают о заданиях. Но на самом деле всё не так страшно, как кажется.
1. Найдите человека, которому вы сможете задавать вопросы
Необязательно нанимать репетитора. Этим человеком может быть учитель в школе или знакомый студент, который учится на химфаке. Главное — не стесняться задавать даже самые глупые, на ваш взгляд, вопросы и стараться закрывать пробелы, которые возникают во время подготовки. Поверьте, то, что у вас появляются хоть какие-то мысли насчёт химии, уже говорит о том, что процесс запущен. Смело поднимайте руку прямо во время урока, расспрашивайте репетитора, участвуйте в обсуждениях в тематических сообществах и не бойтесь выглядеть глупо в глазах других.

2. На экзамене у вас будет три официальные шпаргалки. И в них нужно разбираться
Это таблица Менделеева, таблица растворимости и ряд напряжения металлов. В них содержится около 70% информации, которая поможет вам успешно сдать экзамен. На остальные 30% от вашего успеха приходится ваше умение пользоваться ими.
Чтобы разобраться с таблицей Менделеева, нужно сначала изучить периодические свойства элементов: строение атомов элементов, электроотрицательность, металлические, неметаллические, окислительные и восстановительные свойства, валентности, степени окисления. Если запомните их — не придётся запоминать свойства каждого отдельного элемента или каждого отдельного вещества в природе. Достаточно взглянуть в таблицу и вспомнить о периодическом законе.
Подсказка для тех, кто вечно всё забывает: F (Фтор) самый сильный неметалл и самый электроотрицательный элемент, а Fr (Франций) — наоборот (самый сильный металл и наименее электроотрицательный элемент). Это поможет с чего-то начать.
3. Повторяйте математику. Химию без неё не сдать
Конечно, никто не просит вас интегрировать или дифференцировать и вообще на экзамене можно пользоваться непрограммируемым калькулятором. Но повторить темы процентов и пропорций — обязательно. Формул, которые необходимы для решения задач, не так уж и много. Запомнить нужно только основные: формула для расчёта массовой доли, массы вещества, объёма, количества вещества, плотности и выхода продукта. Зная их, вы сможете без проблем выводить другие.
Попробуйте вывести из формулы массовой доли массу раствора или, зная массу и молярную массу вещества, определить его количество. Через несколько недель тренировок вы заметите, что все эти формулы связаны между собой и, если вы что-то забыли, всегда можно вывести нужную вам формулу из другой.
4. Таблица химических реакций — ваш помощник
Веществ в химии действительно очень много, их можно систематизировать и выявить закономерности. Вам поможет таблица взаимодействия веществ между собой. Распечатайте её и держите перед глазами, когда только начнёте решать цепочки или реакции.
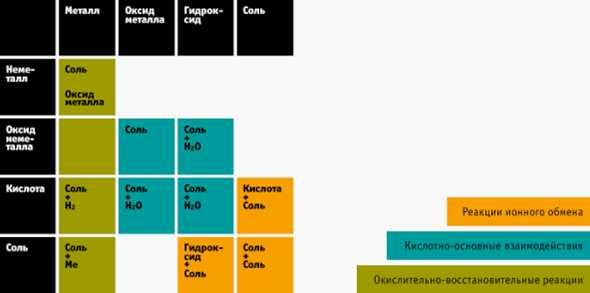 Фото: chemistrytutor.wordpress.com/2008/05/15/inorg
Фото: chemistrytutor.wordpress.com/2008/05/15/inorgКак ей пользоваться?
- Научитесь определять класс веществ (оксиды, кислоты, соли, основания, металлы и неметаллы) и разберитесь в типах реакций, чем они друг от друга отличаются.
- В реакцию вступает минимум два вещества. Определяете, к какому классу относится первое вещество. Находите соответствующий пункт в таблице справа (или вверху).
- Проделайте то же самое со вторым веществом, ищите пункт сверху таблицы (или справа).
- Смотрите на пересечение этих двух пунктов в таблице — это ответ, который получается в реакции.
На экзамене такой шпаргалкой пользоваться нельзя. Но во время подготовки вы легко запомните, что получается, если, например, реагируют кислота и щелочь, и другие вещества. А это около 80% заданий на ЕГЭ.
5. Берите книжки ФИПИ и идите от простого к сложному
На самом деле не важно, какой учебник вы выберете для подготовки к ЕГЭ. Берите тот, где вам будет понятен материал и в котором есть все темы, которые встретятся на экзамене. Что касается тестов, здесь тоже не нужно изобретать велосипед: я рекомендую пользоваться книжками ФИПИ. Тот материал, который они дают, максимально приближен к тому, что будет на экзамене. И можно решать тексты по изученным темам прямо на их сайте.
Начать стоит с блоков, которые встречаются чаще всего:
- строение атома, периодические свойства элементов
- типы химической связи
- классы неорганических веществ
- гидролиз
- электролиз
- взаимодействие веществ между собой и классификация химических реакций
- задачи на тему «растворы»
- химическое равновесие
- органическая химия (классы соединений, их способы получения и химические свойства)
Остальные блоки сложнее. После того, как прорешаете задания по основным блокам, вы поймёте, в каких темах у вас пробелы, а какие вы знаете хорошо. Закрепите темы, которые вы знаете лучше остальных, и вернитесь к изучению теоретической базы тех тем, которые даются хуже. Учите тему и выполняйте по 20 упражнений в день. Если времени для подготовки мало, сосредоточьтесь на заданиях, темы которых вам ясны. Лучше целиком решить задание с ОВР (окислительно-восстановительными реакциями), чем не сделать ничего.

6. Теория хорошо, но без тестов всё равно никуда
Если кажется, что вы всё знаете из теории и вам не нужно тратить время на решение тестов — это не так. Большинство ошибок на экзамене случается из-за того, что ученик неправильно прочитал задание или не понял, что от него хотят. Чем чаще вы будете решать тесты, тем быстрее поймёте структуру экзамена и сложные и загадочные формулировки задания.
Например, в задании № 30 сказано: «Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. В ответе запишите молекулярное, полное и сокращённое ионное уравнения только одной из возможных реакций». Очень часто ученики пропускают стадию написания полного ионного уравнения и пишут сразу сокращённое, потому что так быстрее. Это не ошибка, но за это могу снять один первичный балл.
7. А вот читать лишние статьи и литературу точно не нужно
Иногда во время подготовки к экзамену ученик настолько увлекается, что начинает читать узкоспециализированную литературу. И при ответе на простой вопрос путает самого себя: вроде бы гидроксид цинка проявляет амфотерные свойства и реагирует и с кислотами, и с основаниями, а вот в такой-то статье говорилось, что новые исследования говорят абсолютно о другом. И это ставит под сомнения все фундаментальные знания о химии! Я, конечно, утрирую, но смысл в том, что цель экзамена — проверить ваши знания школьной программы. И стратегия «чем проще, тем вернее» работает в тестах как нельзя лучше.
mel.fm
Готовимся сдавать экзамен по химии – полезные советы
(http://studikam.ru//wp-content/uploads/2012/10/him.jpg)Готовимся сдавать экзамен по химии – полезные советы.
Если вам предстоит сдавать экзамен по химии, мы дадим вам несколько советов, которые, надеемся, помогут получить лучшую оценку. Первое и главное – химия относится к числу тех предметов, которые нельзя выучить за пару дней. Зубрить здесь бесполезно, только понимание предмета поможет вам в сдаче экзамена по химии (http://easyhelp.su/pomowvsdachejekzamenov.html). Поэтому готовимся заранее, без аврала. Упор – на ясное понимание. Для этого лучше заниматься понемногу, но часто. Если пытаешься за день хорошо разобраться сразу в нескольких экзаменационных вопросах, это, бывает, приводит к тому, что вроде хорошо понятый вопрос забывается после того, как разберешься со следующим.
Поэтому в день – два-три вопроса, не больше. Но так, чтобы потом уже не повторять. Если не хватает времени на все вопросы, лучше хорошо разобраться с половиной программы, чем посредственно – со всеми. Учтите, что у большинства преподавателей есть ”любимые” темы, по которым они обычно задают дополнительные вопросы. Эти темы можно узнать от старшекурсников, или у студентов из групп, которые сдают раньше вас. Естественно, их нужно учить в первую очередь. Трудные для запоминания моменты лучше записывать на лист бумаги – и несколько раз, так точно запомните.
Не стоит нагружаться учебой в последний день, и тем более ночь перед экзаменом. Лучше отдохните, сходите с друзьями развеяться. Знания во время отдыха разложатся “по полочкам”, и вы будете лучше соображать, а на экзамене по химии это важнее, чем несколько лишних зазубренных страниц из учебника.
Второе – экзамен по химии – это всегда решение задач. Вы можете не так крепко знать теорию, но если вы умеете решать задачи, удовлетворительная оценка вам практически обеспечена. Поэтому перед экзаменом нужно решать задачи и контрольные работы по химии (http://easyhelp.su/zadachi_po_himii.html) – так много, как только сможете. Потратьте пару дней с репетиром или с понимающим товарищем на разбор задач, а затем сами прорешайте по несколько задач из каждого раздела.
Ну и третье: даже если вы собираетесь честно сдавать экзамен, все равно подготовьте “бомбы” — напишите на листах бумаги краткие ответы на каждый вопрос из программы. Вы можете ими и не воспользоваться, но человек гораздо лучше запоминает то, что написал, чем то, что прочитал. Некоторые преподаватели, когда находят такие бомбы у студентов на экзамене, говорят уважительно – «вижу, что готовился”, и не наказывают.
Удачи вам на экзамене!
studikam.ru
как успешно сдать экзамен по химии. Рекомендации.
Как сдать ЕГЭ по химии?
Химия – не простой, но интересный предмет школьной программы. Он не входит в число обязательных экзаменов, сдают его только те, кто желает продолжить обучение в высшем учебном заведении по специальностям: медицина, химическая или пищевая промышленности и другие отрасли. Выпускники, определившиеся с будущей профессией, должны своевременно начать готовиться к такому сложному предмету, как химия.
Начать подготовку необходимо как можно раньше. Если у Вас есть возможность, то можно записаться на курсы или брать дополнительные уроки у преподавателя, потому что самостоятельно готовиться к данному предмету весьма непросто. Но если вы не можете заниматься платно, придётся серьёзно настроиться на самоподготовку. Будет лучше, есть Вы, уже с 10 класса, начнёте систематизировать информацию необходимую для ЕГЭ.
Теоретические знания крайне важны для написания ЕГЭ по химии, но этого может быть не достаточно для великолепного результата. Обязательно нужно уделить внимание разбору всех тестовых заданий в экзамене. Причём их нужно рассматривать с нескольких позиций и искать альтернативные варианты решения, аргументируя своё мнение. Благодаря этому Вы сможете быстро сориентироваться при написании официального ЕГЭ, и даже встретить подобные задачи.
Рекомендации по подготовке к ЕГЭ
Единый государственный экзамен основан на тестовых технологиях. Такая новая форма экзамена требует хороших знаний по предметам, предварительной психологической подготовки всех участников образовательного процесса (учителей, родителей, учащихся.
Советы учителям:
Учителям, помня о том, что «нельзя научить плавать, стоя на берегу», следует активнее вводить тестовые технологии в систему обучения. В последние годы Центром тестирования РФ выпущены сборники тематических тестов. Эти тесты разработаны для учащихся 5-11 классов практически по всем предметам, выносимым на ЕГЭ. С их помощью можно оценивать уровень усвоения материала учениками и отработать у них навык работы с тестовыми заданиями.
Такие тренировки в выполнении тестовых заданий позволят учащимся в ходе сдачи ЕГЭ реально повысить балл. Зная типовые конструкции тестовых заданий, ученик практически не будет тратить время на понимание инструкции. Во время таких тренировок формируются соответствующие психотехнические навыки само регуляции и самоконтроля.
При этом основную часть работы желательно проводить не перед самим экзаменом, а заранее, отрабатывая отдельные детали при сдаче зачетов по пройденным темам, т.е. в случаях не столь эмоционально напряженных, как сдача ЕГЭ.
Психотехнические навыки, полученные учащимися в процессе обучения, ее только повышают эффективность подготовки к сдаче ЕГЭ, но и позволяют более успешно вести себя во время экзамена, способствуют развитию навыков мыслительной работы, умению мобилизовать себя в решающей ситуации, овладевать собственными эмоциями.
Советы родителям:
Не секрет, что успешность сдачи экзамена во многом зависит от настроя и отношения к этому родителей. Чтобы помочь детям как можно лучше подготовиться к экзаменам, попробуйте выполнить несколько советов:
• Не тревожьтесь о количестве баллов, которые ребенок получит на экзамене. Внушайте ему мысль, что количество баллов не является совершенным измерением его способностей.
• Не повышайте тревожность ребенка накануне экзаменов- это отрицательно скажется на результате тестирования. Ребенок в силу возрастных особенностей может не справиться со своими эмоциями и «сорваться».
• Обеспечьте дома удобное место для занятий, проследите, чтобы никто из домашних не мешал.
• Помогите детям распределить темы подготовки по дням.
• Ознакомьте ребенка с методикой подготовки к экзаменам. Подготовьте различные варианты тестовых заданий по предмету и потренируйте ребенка, ведь тестирование отличается от привычных ему письменных и устных экзаменов.
• Во время тренировки по тестовым заданиям приучайте ребенка ориентироваться во времени и уметь его распределять. Если ребенок не носит часов, обязательно дайте ему часы на экзамен.
• Подбадривайте детей, повышайте их уверенность в себе.
• Контролируйте режим подготовки ребенка к экзаменам, не допускайте перегрузок.
• Обратите внимание на питание ребенка. Такие продукты, как рыба, творог, орехи, курага и т.д. стимулируют работу головного мозга.
• Накануне экзамена обеспечьте ребенку полноценный отдых, он должен отдохнуть и как следует выспаться.
• Не критикуйте ребенка после экзамена.
Помните: главное – снизить напряжение и тревожность ребенка и обеспечить подходящие условия для занятий.
Советы выпускникам:
Подготовка к экзамену
• Подготовьте место для занятий: убери со стола лишние вещи, удобно расположи нужные учебники, пособия, тетради, бумагу, карандаши. Введи в интерьер комнаты желтый и фиолетовый цвета (они повышают интеллектуальную активность). Для этого достаточно картинка или эстампа в этих тонах.
• Составьте план занятий. Для начала определите: кто вы – «сова» или «жаворонок», и в зависимости от этого максимально используйте утренние или вечерние часы.
• Составляя план на каждый день подготовки, необходимо четко определить, что именно сегодня будет изучаться. Не вообще: «немного позанимаюсь», а какие именно разделы и темы.
• Начните с самого трудного раздела, с того материала, который знаете хуже всего. Но если Вам трудно «раскачаться», можно начать с того материала, который наиболее всего интересен и приятен.
• Чередуйте занятия и отдых: 40 минут занятий, 10 минут – перерыв. Во время перерыва можно помыть посуду, полить цветы, сделать зарядку, принять душ. Выполняйте как можно больше опубликованных тестов по этому предмету. Эти тренировки ознакомят Вас с конструкциями тестовых заданий.
• Тренируйтесь с секундомером в руках, засекайте время выполнения тестов (на одно задание в части А в среднем должно уходить не более 2-х минут).
• Готовясь к экзаменам, мысленно рисуйте себе картину триумфа. Никогда не думайте о том, что не справишься с заданием.
• Оставьте один день перед экзаменом на то, чтобы еще раз повторить самые трудные вопросы.
Накануне экзамена
• Многие считают: для того, чтобы полностью подготовиться к экзамену, не хватает всего одной, последней перед ним ночи. Это неправильно. Вы устали, и не надо себя переутомлять. Напротив, с вечера совершите прогулку, перед сном примите душ. Выспитесь как можно лучше, чтобы встать с ощущением «боевого » настроя.
• В пункт сдачи экзамена Вы должны явиться, не опаздывая, лучше за 20 минут до начала тестирования.
• Если на улице холодно, не забудьте тепло одеться, ведь Вы будете сидеть 3-4 часа.
Перед началом экзамена
• В начале тестирования Вам сообщат необходимую информацию (как заполнять бланк, какими буквами писать, как кодировать номер школы и т.д.). Будьте внимательны! От того, как Вы внимательно запомните эти правила, зависит правильность Ваших ответов.
Во время тестирования
• Пробегите глазами весь текст, чтобы увидеть, какого типа задания в нем содержатся.
• Внимательно прочитайте вопрос до конца, чтобы правильно его смысл.
• Если не знаете ответа на вопрос или не уверены, пропустите его, чтобы вернуться потом к нему. Начните с легкого! Начните отвечать на те вопросы, в знании которых Вы не сомневаетесь, не останавливаясь на тех, которые могут вызвать долгие раздумья.
• Научитесь пропускать трудные или непонятные задания. Помните: в тексте всегда найдутся вопросы, с которыми Вы обязательно справитесь
• Думайте только о текущем задании! Когда Вы делаете новое задание, забудьте все, что было в предыдущем. Помните: задания в текстах не связаны друг с другом, поэтому знания, которые Вы применили в одном решенном Вами, как правило, не помогают, а только мешают сконцентрироваться и правильно решить новое задание.
• Многие задания можно быстрее решить, если не искать сразу правильный вариант ответа, а последовательно исключать те, которые явно не подходят. Метод исключения позволяет в итоге сконцентрировать внимание всего на одном-двух вариантах, а не на пяти-семи.
• Оставьте время для проверки своей работы, чтобы успеть пробежать глазами и заметить явные ошибки.
• Если не уверены в выборе ответа, доверьтесь интуиции.
Методические рекомендации для уроков обобщения и повторения при подготовке к ОГЭ и ЕГЭ по химии.
Практика показывает, что учитель не может обеспечить полностью подготовку учащихся 9-х классов к ОГЭ и 11-х классов к ЕГЭ по химии на уроках, особенно при 1 или 2-х часовом изучении этого предмета в неделю.
Однако учитель может оказать большую помощь учащимся, придерживаясь определённой методики.
1.Повторение. Это одна из самых важных частей подготовки к экзаменам.
Не нужно откладывать организацию повторения на конец учебного года. Чем раньше учитель начнёт совмещать организацию повторения на уроке с изучением нового материала, те лучше будет результат. Не обязательно выделять повторение на уроке в отдельный блок. На это может не хватить времени. Повторяйте пройденные темы при опросе учащихся, связывайте новый материал с ранее изученным и даже при закреплении новой темы.
Без повторения рассчитывать на высокие результаты при сдаче ЕГЭ не приходится.
0рганизацию повторения нужно внести в календарно- тематическое планирование. Невозможно повторить за несколько месяцев весь пройденный материал. К тому же у каждого ребёнка свои пробелы в знаниях. Учитель должен определить основные темы, по которым учащиеся испытывают трудности.
Нельзя пользоваться проверочными тестами только одного автора или издания. Выпускник должен быть готов справиться с любым заданием, как бы не был сформулирован вопрос.
Кроме того, для каждого ученика можно составить индивидуальную программу для повторения . Но выполнять её он должен самостоятельно. У каждого ученика свои слабые места, потому и акценты будут расставлены по-разному.
Самые распространенные ошибки учеников:
1.Механизмы образования связи. Затруднения в выборе веществ, имеющих связь, образованную по донорно-акцепторному механизму: если в ответе есть соль аммония, ошибок нет, но если следует выбрать озон, угарный газ, комплексное соединение – верных ответов гораздо меньше.
2.Водородная связь. Обязательно следует напомнить классы органических соединений, которые образуют этот вид связи, вспомнить ее влияние на физические свойства.
Часто учащиеся ошибочно считают, что вещества, имеющие ионные кристаллические решетки проводят электрический ток в твердом состоянии, забывая о прочности ионной связи, и, как следствие, о невозможности свободного перемещения ионов.
3.Закономерности протекания химических реакций
. При повторении химической кинетики надо обратить внимание на факторы, влияющие на скорость реакции. Часто, если в вопросе о скорости реакции авторы пособий
уравнении поставили знак обратимости ⇆ , этого достаточно, чтобы подтолкнуть ученика к неверному ответу, в котором он, вместо факторов, влияющих на скорость , рассматривает факторы, влияющие на равновесие.
При повторении химического равновесия чаще других встречается ошибка, когда рассматривается влияние давления на равновесие и суммируется количества веществ – газов и твердых веществ или газов и жидкостей. Для запоминания того, что объемами жидкостей и твердых веществ в данном случае можно пренебречь, можно сравнить объем 1 моля водяных паров (22400мл) и объем 1 моль жидкой воды (18 мл).
4.Физико-химические свойства растворов. Электролитическая диссоциация. Реакции в растворах электролитов
Уравнения ступенчатой диссоциации многоосновных кислот, многокислотных оснований, а также кислых, основных и комплексных солей. Очень часто встречается ошибка в записи диссоциации кислых солей:
NaHS⇆Na+ + Н+ + S ² ˉ
Обратите внимание на факторы, влияющие на степень диссоциации слабых электролитов. 5. Влиянии разбавления раствора на степень диссоциации (закон разведения Оствальда). Формулировка самого вопроса в тестах «Яркость свечения лампочки усилится…» не всем ученикам понятна.
6.Гидролиз солей
О среде в растворах дигидрофосфатов и гидросульфитов.
О взаимном усилении гидролиза, например, при смешивании растворов хлорида железа (III) и карбоната натрия.
Укажите, что при смешивании солей железа (III) с сульфидами, происходит не взаимное усиление гидролиза, а ОВР.
Необходимо повторить и необратимый гидролиз бинарных соединений (карбидов, силицидов, нитридов, фосфидов, активных металлов).
7.Амфотерные соединения.
Повторите темы, касающиеся продуктов реакций амфотерных оксидов и гидроксидов в растворе и при сплавлении.
Обратите внимание ученика на степень окисления амфотерного металла и зависимость от нее продукта реакции.
Повторите разрушение гидроксокомплексов в кислой среде. Обратите внимание на разрушение их продуктами гидролиза солей слабых оснований и сильных кислот ( к комплексу добавляют раствор соли алюминия, цинка, железа).
8.Основные классы соединений. Обратить особое внимание на зависимость продуктов реакции от избытка-недостатка реагентов: например, при взаимодействии щелочей с оксидом углерода (IV) может образоваться как средняя, так и кислая соль.
Обязательно уделите внимание вопросу о термической устойчивости, особенно нитратов.
Напомните ученикам различия между промышленными способами получения веществ и лабораторными. Не забывайте заострить внимание на том, что такое оптимальные условия получения.
Повторите качественные реакции на вещества и ионы.
Для успешной подготовки учащихся к ЕГЭ учителю рекомендуется реализовать предлагаемый алгоритм:
1. Анализ информации по содержанию и процедуре проведения ЕГЭ.
1.1.Выявить число учащихся, предполагающих сдавать ЕГЭ по химии.
1.2.Познакомиться с нормативными документами, регламентирующими содержание и процедуру проведения ЕГЭ (опубликованы на сайтах www.ege.edu.ru, www.fipi.ru, www.educom.ru, www.mioo.ru, ege.flpi.org)
1.З.Согласовать с руководством образовательного учреждения организационную форму подготовки учащихся к ЕГЭ (консультационные часы, факультатив, спецкурс и т.п.).
1.4.Проанализировать содержание ЕГЭ по спецификации
1.5.Проанализировать учебно-методическое обеспечение (учебники, дополнительная литература, сборники тестов, интернет-сайты) для подготовки учащихся к ЕГЭ.
2.Выявить уровень усвоения учащимися всех тем курса в процессе проведения пробного тестирования по материалам демонстрационной версии ЕГЭ.
3.Составить календарно-тематическое планирование, отражающее темы занятий, их содержание, перечень основных знаний и умений, перечень обязательной номенклатуры. Календарно-тематическое планирование составляется с учетом количества часов и сроков, выделенных на подготовку к ЕГЭ.
4.В календарно-тематическое планирование необходимо внести сроки и формы диагностики уровня усвоения повторяемого материала.
5.При планировании повторения рекомендуется учитывать уровень индивидуальной подготовки учащихся. Для этого следует разработать индивидуальные планы подготовки учащихся к ЕГЭ, и согласовать их с учениками и их родителями.
6.Рекомендуется включить в план знакомство учащихся с оформлением бланков ответов ЕГЭ.
7.В процессе занятий рекомендуется не только повторение теоретических вопросов, но и практическая отработка материала.
infourok.ru
Как сдать экзамен по химии Как? Так!
Содержимое:
5 метода:
Чтобы успешно сдать экзамен по общей химии, важно знать основы предмета, уметь считать, использовать калькулятор для более сложных задач и быть готовым узнать что-то новое. Химия изучает вещества и их свойства. Все вокруг нас связано с химией, даже простейшие вещи, которые мы принимаем как должное, – например, вода, которую мы пьем, и воздух, которым мы дышим. Будьте готовы к открытиям обо всем, что вас окружает. Знакомство с химией будет увлекательным.
Шаги
Метод 1 Полезные привычки в учебе
- 1 Познакомьтесь с преподавателем или учителем. Чтобы успешно сдать экзамен, следует познакомиться с преподавателем и рассказать ему, что вам дается с трудом.
- Ко многим преподавателям можно подойти вне уроков, если студентам нужна помощь. Кроме того, у них обычно есть методические издания.
- 2 Соберите группу для занятий. Не стесняйтесь того, что химия дается вам тяжело. Этот предмет сложен практически для всех.
- Работая в группе, люди, которые смогут быстро понять какую-то тему, объяснят ее остальным. Разделяйте и властвуйте.
- 3 Прочитайте нужные параграфы в учебнике. Учебник по химии – не самое захватывающее чтиво, но вам следует внимательно ознакомиться с материалом и выделить текст, который вам не понятен. Составьте список вопросов и понятий, которые вам сложно понять.
- Вернитесь к этим частям позже со свежей головой. Если вам все равно трудно, обсудите тему в группе или обратитесь за помощью к преподавателю.
- 4 Ответьте на вопросы после параграфа. Даже если материала много, вы, возможно, запомнили больше, чем вам кажется. Постарайтесь ответить на вопросы в конце главы.
- Иногда в учебниках есть поясняющие материалы в конце, которые описывают правильное решение. Это поможет вам понять, где вы совершили ошибку в рассуждениях.
- 5 Изучите диаграммы, изображения и таблицы. В учебниках используются наглядные способы передачи информации.
- Посмотрите на изображения и схемы. Это позволит лучше понять некоторые концепции.
- 6 Попросите у преподавателя разрешения записывать лекцию на диктофон. Сложно записывать информацию и при этом смотреть на доску, особенно если речь идет о таком непростом предмете, как химия.
- 7 Ознакомьтесь с вопросами прежних экзаменов. Иногда студентам выдают вопросы, которые встречались на экзаменах в прошлые годы, чтобы они могли лучше подготовиться.
- Не заучивайте ответы. Химия – это предмет, где для ответа на вопрос важно понимать, о чем идет речь, а не только повторять заученный текст.
- 8 Воспользуйтесь учебными онлайн-ресурсами. Посетите все сайты, которые рекомендует преподаватель.
Метод 2 Понимание атомистического строения
- 1 Начните с самого простого строения. Чтобы стать экзамен, вам нужно будет знать, из чего состоит все, что является веществом и обладает массой.
- Все начинается с понимания строения атома. Все остальное будет добавляться сверху. Важно очень тщательно изучить всю информацию об атоме.
- 2 Ознакомьтесь с концепцией атома. Атом – это мельчайших “кирпичик” всего, у чего есть масса, включая вещества, которые мы не всегда можем увидеть (к примеру, газы). Но даже в атоме есть мельчайшие частицы, которые формируют его структуру..
- Атом состоит из трех частей – нейтроны, протоны и электроны. Центр атома называется ядром. Ядро состоит из нейтронов и протонов. Электроны – это частицы, которые вращаются вокруг внешней оболочки атома как планеты вокруг солнца.
- Атом очень маленький. Представьте себе самый большой стадион из всех известных вам. Если стадион – это атом, то ядро этого атома имеет размер горошины.
- 3 Узнайте, что представляет собой атомная структура элемента. Элемент – это вещество в природе, которое нельзя расщепить на более мелкие вещества. Элементы состоят из атомов.
- Атомы в элементе не меняются. Это означает, что у каждого элемента есть определенное уникальное число нейтронов и протонов в его атомной структуре.
- 4 Выясните, как устроено ядро. Нейтроны в ядре обладают нейтральным зарядом. У протонов положительный заряд. Атомное число элемента равняется количеству протонов в ядре..
- Нет необходимости считать количество протонов в ядре. Это число указывается в периодической таблице химических элементов для каждого элемента.
- 5 Посчитайте количество нейтронов в ядре. Можно использовать число из периодической таблицы. Атомное число элемента совпадает с количеством протонов в ядре.
- Атомная масса указывается внизу квадрата каждого элемента под его названием.
- Помните, что в ядре атома есть лишь протоны и нейтроны. В периодической системе указано количество протонов и значение атомной массы.
- Теперь посчитать все будет просто. Отнимите количество протонов от атомной массы, и вы получите количество нейтронов в ядре каждого атома элемента.
- 6 Посчитайте количество электронов. Помните, что частицы с противоположными зарядами притягиваются. Электроны имеют положительный заряд и крутятся вокруг атома. Количество негативно заряженных электронов, которые притягиваются к ядру, зависит от количества положительно заряженных протонов в ядре.
- Поскольку сам атом обладает нейтральным зарядом, количество частиц с отрицательным зарядом должно равняться количеству частиц с положительным зарядом. По этой причине количество электронов равняется количеству протонов.
- 7 Обратитесь к периодической системе элементов. Если вам трудно даются свойства элементов, изучите всю доступную информацию о периодической таблице.
- Понимание периодической таблицы важно для успешной сдачи экзамена.
- Периодическая система состоит только из элементов. У каждого элемента есть буквенный символ, этот символ всегда обозначает этот элемент. К примеру, Na – это всегда натрий. Полное название элемента размещается под буквенным символом.
- Число над буквенным символом – это атомное число. Оно равняется количеству протонов в ядре.
- Число под буквенным символом – это атомная масса. Помните, что атомная масса – это сумма протонов и нейтронов в ядре.
- 8 Научитесь читать таблицу. В таблице много информации, от цветов колонок до расположения элементов слева направо и сверху вниз.
Метод 3 Расчет химических реакций
- 1 Напишите уравнение. На занятиях по химии вас будут учить определять, что произойдет с элементами при их соединении. На бумаге это называется решением уравнения.
- Химическое уравнение состоит из веществ с левой стороны, стрелочки и продукта реакции. Вещества с одной стороны уравнения должны уравновешивать вещества с другой стороны.
- Например, вещество 1 + вещество 2 → продукт 1 + продукт 2.
- Возьмем олово (Sn) в окисленной форме (SnO2) и соединим с водородом в форме газа (h3). SnO2 + h3 → Sn + h3O.
- Это уравнение необходимо балансировать, поскольку количество веществ-реагентов должно равняться количеству полученных продуктов. В левой части больше атомов кислорода, чем в правой.
- Подставим две единицы водорода слева и две молекулы воды справа. В финальной версии сбалансированное уравнение выглядит так: SnO2 + 2 h3 → Sn + 2 h3O.
- 2 Подумайте об уравнениях по-новому. Если вам сложно балансировать уравнения, представьте, что это рецепт, но его нужно скорректировать с обеих сторон.
- В задании вам даны ингредиенты с левой стороны, но не сказано, сколько их нужно брать. В уравнении также сказано, что получится, но не сказано, в каких количествах. Вам нужно выяснить это.
- На примере предыдущего уравнения, SnO2 + h3 → Sn + h3O, подумаем, почему такая формула не будет работать. Количество Sn равно с двух сторон, как и количество h3, однако слева две части кислорода, а справа – лишь одна.
- Необходимо изменить правую часть уравнения так, чтобы в полученном продукте было две части h3O. Двойка перед h3O означает, что все количества будут увеличены в два раза. Теперь кислород сбалансирован, однако двойка означает, что справа теперь больше водорода, чем слева. Вернитесь к левой части и увеличьте водород в два раза, поставив перед ним двойку.
- Теперь все уравновешено. Количества на входе равны количествам на выходе.
- 3 Добавьте больше деталей в уравнение. На занятиях по химии вы познакомитесь с символами, которые обозначают физическое состояние элементов: т – твердое, г – газ, ж – жидкость.
- 4 Научитесь определять изменения, которые происходят при химической реакции. Химические реакции начинаются с базовых элементов или соединений, которые вступают в реакцию. В результате соединения получается продукт реакции или несколько продуктов.
- Чтобы сдать экзамен, нужно знать, как решать уравнения, в которых содержатся реактанты или продукты соединений либо и то, и другое.
- 5 Выучите разные типы реакций. Химические реакции могут происходить под воздействием различных факторов, а не только при соединении элементов.
- К наиболее распространенным типам реакций относятся синтез, анализ, замещение, двойное разложение, реакция между кислотами и основаниями, окисление-восстановление, горение, изомеризация, гидролиз.
- На занятиях могут изучаться разные реакции – все зависит от целей курса. В университете степень углубления в материал будет отличаться от школьной программы.
- 6 Используйте все доступные ресурсы. Вам нужно будет понять разницу между основными реакциями. Используйте все возможные материалы, чтобы понять эту разницу. Не бойтесь задавать вопросы.
- Понять, что меняется при химических реакциях, не так просто. Это будет одной из самых сложных задач на занятиях по химии.
- 7 Осмыслите реакции с точки зрения логики. Постарайтесь не запутаться в терминологии и не сделать все еще сложнее. Все реакции направлены на превращение чего-то во что-то другое.
- К примеру, вы уже знаете, что получится, если соединить два атома водорода и один атом кислорода, – вода. Поэтому если налить воду в кастрюлю и поставить на огонь, что-то изменится. Вы провели химическую реакцию. Если поставить воду в холодильник, произойдет реакция. Вы изменили что-то, что задействовало вещество, участвующее в реакции, то есть воду.
- Пройдитесь по каждому типу реакции, пока не поймете все. Сконцентрируйтесь на источнике энергии, который провоцирует реакцию, и основных изменениях, которые становятся результатом реакции.
- Если вам сложно разобраться в этом, составьте список непонятных нюансов и покажите его преподавателю, сокурсникам или любому человеку, который хорошо разбирается в химии.
Метод 4 Расчеты
- 1 Знайте последовательность основных вычислений. В химии иногда нужны очень точные расчеты, но часто достаточно базовых знаний математики. Важно понимать, в какой последовательности осуществляются расчеты.
- Сначала делаются расчеты в скобках, затем вычисления в степенях, затем умножение или деление и в конце – сложение или вычитание.
- В примере 3 + 2 x 6 = ___ правильным ответом будет 15.
- 2 Не бойтесь округлять очень длинные числа. В химии часто округляют, потому что нередко ответом на уравнение служит число с большим количеством цифр. Если в условии задачи даны инструкции по округлению, учтите их.
- Знайте, как округлять. Если следующая цифра – это 4 или меньше, следует округлять к меньшему, если 5 и больше 5 – к большему. Например, перед вами число 6.66666666666666. В задании сказано округлить ответ до второй цифры после точки. Ответом будет 6.67.
- 3 Поймите, что такое абсолютное значение. В химии у некоторых чисел есть абсолютное, а не математическое значение. Абсолютное значение – это все значения до числа от нуля.
- Иными словами, у вас больше нет отрицательных и положительных значений, есть только расстояние до нуля. К примеру, абсолютным значением -20 является 20.
- 4 Знайте все распространенные единицы измерения. Вот несколько примеров.
- Количество вещества измеряется в молях (mol).
- Температура измеряется в градусах по Фаренгейту (°F), Кельвину (°K) или Цельсию (°C).
- Масса измеряется в граммах (г), килограммах (кг) или в миллиграммах (мг).
- Объем жидкости измеряют в литрах (л) или миллилитрах (мл).
- 5 Потренируйтесь переводить значения из одной системы измерения в другую. На экзамене вам придется заниматься такими переводами. Возможно, вам нужно будет перевести температуру из одной системы в другую, фунты – в килограммы, унции – в литры.
- Вас могут попросить дать ответ в единицах, отличных от единиц в условии задачи. К примеру, в тексте задачи температура будет указана в градусах по Цельсию, а ответ нужен будет в градусах по Кельвину.
- Обычно температуру химических реакций измеряют в градусах по Кельвину. Потренируйтесь переводить градусы по Цельсию в градусы по Фаренгейту или Кельвину.
- 6 Не спешите. Вдумчиво прочитайте текст задачи и научитесь переводить единицы измерения.
- 7 Умейте рассчитывать концентрацию. Отточите знания основ математики, рассчитывая проценты, соотношения и пропорции.
- 8 Попрактикуйтесь на данных о пищевой ценности продуктов на упаковках. Чтобы сдать химию, вам нужно уметь рассчитывать соотношения, пропорции и проценты в разных последовательностях. Если вам это сложно, начните тренироваться на привычных единицах измерения (к примеру, на упаковках пищевых продуктов).
- Возьмите упаковку с данными о пищевой ценности. Вы увидите расчет калорий на порцию, рекомендуемую порцию продукта в день в процентах, общее количество жира, процент калорий от жира, общее количество углеводов и разбивку по типам углеводов. Научитесь высчитывать различные соотношения, отталкиваясь от этих значений.
- Например, рассчитайте количество мононенасыщенного жира в общем количестве жиров. Переведите в процентное соотношение. Рассчитайте, сколько калорий содержится в упаковке, зная количество порций и калорийность каждой порции. Рассчитайте, сколько натрия содержится в половине упаковки.
- Это поможет вам с легкостью переводить химические значения из одной системы в другу, например, моли на литр, граммы на моль и так далее.
- 9 Научитесь использовать число Авогадро. Это число отражает количество молекул, атомов или частиц в одном моле. Постоянная Авогадро равняется 6.022×1023.
- Например, сколько атомов в 0.450 молях Fe? Ответ: 0.450 x 6.022×1023.
- 10 Подумайте о морковке. Если вам сложно понять, как использовать число Авогадро, попробуйте считать морковь, а не атомы, молекулы или частицы. Сколько морковок содержится в дюжине? Мы знаем, что дюжина – это 12, значит, в одной дюжине 12 морковок.
- Теперь ответим на вопрос, сколько морковок содержится в моле. Вместо того чтобы умножить на 12, мы умножим на число Авогадро. В моле 6.022 x 1023 морковок.
- Число Авогадро используется для конвертации любого значения атомов, молекул, частиц или морковок в моли.
- Если вы знаете количество молей вещества, значит, значение числа молекул, атомов или частиц будет равняться этому числу, умноженному на число Авогадро.
- Понимание того, как частицы переводятся в моли, – важный фактор на экзамене. Конвертации в моли – это часть расчетов соотношений и пропорций. Это означает количество чего-то в молях как часть чего-то еще.
- 11 Разберитесь в молярности. Подумайте о количестве молей вещества, содержащегося в жидкости. Очень важно понять этот пример, поскольку речь идет о молярности, то есть о пропорции вещества, выраженного в молях на литр.
- Молярность, или молярная концентрация, – это термин, который выражает количество какого-то вещества в жидкости, то есть количество растворенного вещества в растворе. Чтобы получить молярность, нужно разделить моли растворенного вещества на литры раствора. Молярность выражается в молях на литр.
- Рассчитайте плотность. Плотность часто используется в химии. Плотность – это масса химического вещества на единицу объема. Обычно плотность выражается в граммах на миллилитр или в граммах на кубический сантиметр – это то же самое.
- 12 Сведите уравнения к эмпирической формуле. Это означает, что ответ будет верным лишь в том случае, если вы доведете все значения до их простейшей формы.
- Это не касается молекулярных формул, поскольку в них указываются точные пропорции химических элементов, входящих в молекулу.
- 13 Знайте, что включается в молекулярную формулу. Молекулярную формулу не нужно доводить до простейшей, или эмпирической, формы, поскольку в ней сказано, из чего именно состоит молекула.
- Молекулярная формула записывается с помощью аббревиатур элементов и количества атомов каждого элемента в молекуле.
- К примеру, молекулярная формула воды – это h3O. Это означает, что в каждой молекуле воды содержится два атома водорода и один атом кислорода. Молекулярная формула ацетаминофена – C8H9NO2. У каждого химического соединения есть молекулярная формула.
- 14 Помните, что математика в химии называется стехиометрией. Вы встретите этот термин. Это описание того, как химия выражается в математических формулах. В химической математике, или в стехиометрии, количества элементов и химических соединений часто выражаются в молях, процентах в молях, в молях на литр или в молях на килограмм.
- Вам нужно будет переводить граммы в моли. Атомная масса единицы элемента в граммах равняется одному молю этого вещества. К примеру, атомная масса кальция – 40 единиц атомной массы. Таким образом, 40 граммов кальция равняются одному молю кальция.
- 15 Попросите о дополнительных заданиях. Если вам тяжело даются уравнения и конвертации, поговорите с преподавателем. Попросите дать вам больше задач, чтобы вы могли поработать над ними самостоятельно, пока суть всех явлений не станет вам понятна.
Метод 5 Язык химии
- 1 Научитесь понимать диаграммы Льюиса. Диаграммы Льюиса иногда называют точечными диаграммами. Это простые схемы, на которых точками обозначаются свободные и связанные электроны во внешней оболочке атома
- Такая система позволяет нарисовать простые диаграммы, на которых были бы отражены связи между элементами в атоме или молекуле, к примеру, ковалентные.
- 2 Узнайте, что такое правило октетов. При построении диаграмм Льюиса используется правило октетов, которое гласит, что атом становится стабильным, когда у него есть доступ к восьми электронам во внешней оболочке. Водород является исключением – он считается стабильным при наличии двух электронов во внешней оболочке.
- 3 Нарисуйте диаграмму Льюиса. Буквенный символ элемента в окружении точек и является диаграммой Льюиса. Представьте, что диаграмма – это рамка кинофильма. Электроны не вращаются вокруг внешней оболочки элементы – они отражены в определенном отрезке времени.
- На диаграмме изображается неподвижная масса электронов, места их соединения с другим элементом и информация о связи (например, удваиваются ли связи и делятся ли они между несколькими электронами).
- Подумайте о правиле октетов и представьте символ элемента – к примеру, С (углерод). Нарисуйте по две точки на востоке, западе, севере и юге символа. Теперь нарисуйте символ Н (атом водорода) с каждой стороны каждой из точек. На диаграмме видно, что каждый атом углерода окружен четырьмя атомами водорода. Их электроны связаны ковалентно, то есть у атомов углерода и водорода один из электронов связан с электроном второго элемента.
- Молекулярная формула такого соединения – Ch5. Это газ метан.
- 4 Разберитесь в том, как электроны связывают элементы. На диаграммах Льюиса в простой форме представлены химические связи.
- Обсудите эту тему с преподавателем и одногруппниками, если вам непонятно, как связываются элементы и что отражают диаграммы Льюиса.
- 5 Узнайте, как называются соединения. В химии есть свои правила терминологии. Типы реакций, потеря или приобретение электронов во внешней оболочке и стабильность либо нестабильность элементов являются частью терминологии химии.
- 6 Подойдите к этому серьезно. Во многих курсах по химии этому выделяют отдельные главы. Нередко незнание терминологии означает несдачу экзамена.
- По возможности изучите терминологию до занятия. Можно купить специальную литературу в обычном книжном магазине или в интернете.
- 7 Знайте, что означают цифры над и под строкой. Это очень важная часть изучения химии.
- Цифры над строкой можно видеть в периодической системе элементов. Они означают общий заряд элемента или химического соединения. Изучите периодическую систему и элементы в вертикальных рядах, у которых одинаковые индексные цифры.
- Цифры внизу строки используются для описания количества каждого элемента, который входит в соединение. Как было сказано раньше, 2 в формуле h3O говорит о том, что в молекуле воды есть два атома водорода.
- 8 Поймите, как атомы реагируют друг с другом. В терминологии есть специальные правила, которыми следует руководствоваться, называя продукты определенных типов реакций.
- Одной из реакций является окисление-восстановление. В процессе реакции происходит либо приобретение, либо потеря электронов.
- Электроны теряются при окислении и приобретаются при восстановлении.
- 9 Помните, что числа внизу строки могут указывать на формулу стабильного заряда соединения. Ученые используют такие числа, чтобы описать конечную молекулярную формулу соединения, а это также обозначает стабильное соединение с нейтральным зарядом.
- Чтобы получить нейтральный заряд, позитивно заряженный ион, который называется катионом, должен быть уравновешен равным зарядом от негативного иона – аниона. Эти заряды пишутся внизу строки.
- Например, в ионе магния +2 заряд катиона, а в ионе азота -3 заряд аниона. +2 и -3 указываются внизу строки. Чтобы получить нейтральный заряд, на каждые 2 единицы азота нужно использовать 3 атома магния.
- В формуле это записывается так: Mg3N2
- 10 Научитесь узнавать анионы и катионы по их положению в периодической таблице элементов. Элементы таблицы, которые находятся в первой колонке, являются щелочными металлами, и у них +1 заряд катионов. Например, Na+ and Li+.
- Щелочно-земельные металлы во второй колонке обладают зарядом 2+ катионов, например, Mg2+ и Ba2+.
- Элементы в седьмой колонке называются галогенами, и у них заряд -1 анионов, к примеру, Cl- и I-.
- 11 Научитесь узнавать распространенные анионы и катионы. Чтобы сдать экзамен, изучите всю терминологию, связанную с группами элементов. Эти числа внизу строки не меняются.
- Иными словами, магний – это всегда Mg с зарядом катионов +2.
- 12 Постарайтесь не запутаться в информации. Через вас будет проходить информация о разных типах химических реакций, об обмене электронами, о смене заряда элемента или его составляющего, и все это будет сложно усвоить.
- Разбейте сложные темы на части. Например, если вы не понимаете реакции окисления или принцип сочетания элементов с положительным и отрицательным зарядами, начните проговаривать всю известную вам информацию, и вы поймете, что вы уже успели понять и запомнить многое.
- 13 Регулярно общайтесь с преподавателем. Составьте список сложных тем и попросите преподавателя помочь вам. Это даст вам возможность усвоить материал до того, как группа перейдет к следующей теме, что еще больше запутает вас.
- 14 Представьте, что химия – это как учить новый язык. Важно понять, что письменное обозначение зарядов, количества атомов в молекуле и связи между молекулами – это часть языка химии. Все это отражает то, что происходит в природе, на бумаге.
- Было бы гораздо проще понять все это, если бы все процессы можно было бы наблюдать вживую. Вам важно не только понимать принципы процессов, но и язык, который используется для записи этой информации.
- Если вам сложно изучать химию, помните, что вы одни, и не сдавайтесь. Поговорите с преподавателем, с группой или с любым человеком, который хорошо разбирается в этом предмете. Все это можно выучить, но было бы более правильно, если бы кто-нибудь смог объяснить вам материал так, чтобы вы все поняли.
Советы
- Не забывайте отдыхать. Если отвлечься от занятий, это позволит вам вернуться к учебе со свежей головой.
- Накануне экзамена выспитесь. У выспавшегося человека лучше работает память и концентрация внимания.
- Перечитайте то, что вы уже знаете. Химия – это наука, построенная на изучении одного явления и расширении знаний. Важно удерживать все выученное в памяти, чтобы вопрос на экзамене не удивил вас.
- Готовьтесь к занятиям. Читайте все материалы и выполняйте домашнюю работу. Вы будете отставать все больше и больше, если упустите что-то.
- Распределите время. Уделите химии больше внимания, если этот предмет вам плохо дается, но не посвящайте ей все время, потому что есть и другие предметы.
Прислал: Калинина Инна . 2017-11-11 19:24:57
kak-otvet.imysite.ru
Как сдать ЕГЭ по химии: советы и рекомендации
Единый государственный экзамен (ЕГЭ) по химии не относится к перечню обязательных. Сдавать химию стоит лишь в том случае, если ваш выбор будущей профессии лежит в области медицины, строительства, химических или биотехнологий.
Часто школьники задают педагогам вопрос: «Сложно ли сдавать ЕГЭ по химии?» Ответить на него однозначно непросто, но узнать об экзаменационном процессе чуть больше стоит каждому, кто выбрал эту дисциплину.
Экзамен состоит из 40 заданий, которые делятся на три части – А, В и С.
Выполнение части А: ошибки и советы
Задания А1-А26 относятся к базовому уровню, а правильный ответ на каждый вопрос приносит ученику один первичный балл.  Предлагается четыре варианта ответов, из которых нужно выбрать один правильный.
Предлагается четыре варианта ответов, из которых нужно выбрать один правильный.
Рассмотрим, как решать эти типы заданий.
| Тип задания | Возможная ошибка | Действие |
| Стандартный простой вопрос | Поспешный ответ |
Дочитайте весь вопрос до конца, отбросьте явно неверные варианты и выберите правильный ответ |
| Вопрос с отрицанием | Ответ на вопрос с точностью до наоборот |
Не забывайте об отрицании |
|
Выбор группы |
Акцентирование внимания на первом вещ-ве в группе | Условию задачи должны отвечать все перечисленные в группе элементы |
|
Два суждения |
Незнание некоторых исключительных свойств того или иного вещ-ва |
Вспомните правила-исключения из химии |
 Общие рекомендации:
Общие рекомендации:
- решайте задания в три этапа: на первом отбрасывайте трудные вопросы и решайте только очевидные; на втором – думайте и вспоминайте правила-исключения; а на третьем, если остались нерешенные задания – подключайте интуицию и постарайтесь угадать правильный ответ;
- помните о шпаргалках: периодической системе, таблице растворимости и ряде напряжения;
- если вам кажется, что в перечне ответов есть несколько правильных вариантов, перечитайте их несколько раз: возможно, вы пропустили отрицание или факты, которые в принципе возможны, но на практике не используются;
- помните об особых свойствах некоторых веществ и исключениях из правил.
Выполнение части В: углубляемся и сосредотачиваемся
В1-В9 – так маркируются задания повышенного уровня сложности, где необходимо записать краткий ответ. Каждое выполненное задание оценивается от 1 до 2 баллов, а в сумме за правильно выполненные задания можно получить 18 первичных баллов.
Здесь есть градация заданий по типам, и, соответственно, свои нюансы выполнения.
| Тип задания | Возможная ошибка | Действие |
|
Задания на соответствия |
Стремление применить каждый предложенный вариант ответа | Внимательно перечитайте каждый предложенный вариант ответа. Учтите, что буквы в ответе могут повторяться, а часть предложенных вариантов может быть не применима для решения задачи |
|
Выбор группы |
Запутаться в названиях соединений каждой группы из-за необходимости сопоставлять сразу несколько параметров |
Для правильного ответа необходимо учитывать взаимодействия вещ-в. Здесь может помочь отбрасывание ненужных вариантов |
|
Соответствия между веществами и коэффициентом ионного уравнения |
Забыть о коэффициенте 1, который не пишется. При переходе от полного ионного уравнения к сокращенному многие забывают, что можно сокращать и коэффициенты, если их можно разделить на одно и то же число. |
Помните о правилах решения ионных уравнений, о сокращении коэффициентов. Не путайте нумерацию вариантов ответов со значениями ответов |
| Задания с множественным выбором |
Использование только одного варианта или сразу всех. Запись выбранных вариантов в хаотичном порядке |
Помните, что есть специальное поле для предварительных расчетов, и только после того, как вы окончательно решите задание, запишите в бланк ответа варианты в порядке их возрастания. Как правило, в этом типе заданий 3 правильных варианта ответа |
| Расчетные задачи | Ошибки при округлении | Используйте поле для расчетов и записывайте только верный ответ |
Общие советы для решения задач части В:
- не спешите с записью ответов в контрольный бланк;
- если вы сомневаетесь в задании с множественным выбором, то лучше напишите меньшее количество вариантов ответов.

Часть С: максимум внимания
Задания самого сложного уровня ЕГЭ по химии – С1-С5. Их всего пять, для каждого необходимо дать полный развернутый ответ. Задачи оцениваются в 3 или 4 балла, а максимум, который можно получить за всю часть С – 18 баллов.
Если «застрянете» на первых двух частях, то на решение третьей у вас не хватит времени. Посмотрите на основные типы заданий в части С и те ошибки, которые чаще всего допускают ученики.
| Тип задания | Возможная ошибка | Действие |
| Уравнения окислительно-восстановительной реакции | Даже при правильном решении уравнения многие забывают указать окислитель-восстановитель | Определите недостающие вещ-ва реакции и степень окисления, примените стандартный алгоритм электронного баланса. Перепроверьте данный вами ответ |
| Уравнения возможных реакций для набора неорганических веществ | Многие забывают перепроверить записанный ответ | Записывайте только те уравнения, в которых вы уверены на 100%, т. к. засчитываются только первые 4 |
| «Мысленный эксперимент» | Некоторые экзаменуемые пропускают эту задачу в виду неясности ответа | 1) составьте схему реакции; 2) расшифруйте схему, заменив обозначения конкретными формулами; 3) напишите уравнения реакций, расставив все коэффициенты. Сделайте хотя бы один из перечисленных шагов правильно, и это принесет вам балл |
| Цепочка превращений органических веществ |
Не указать помимо основных продуктов побочные. Экзаменуемые не учитывают условия протекания реакции и записывают уравнения без структурных формул |
Учитывайте последовательность протекания реакций, правильно записывайте формулы. Помните о сложных реакциях (окисление перманганатом, электролиз растворов солей карбоновых кислот, взаимодействие галогенпроизводных со спиртовым и водным раствором щелочи и т. д.) |
| Комбинированная задача | Ошибки в номенклатуре, уравнениях реакций. Часто экзаменуемые не понимают разницу между фосфатом и фосфидом, нитритом и нитридом | Записывайте все результаты реакций на каждом этапе решения задачи и учитывайте их в последующих расчетах по уравнению реакции |
| Определение формулы вещества | В задачах на продукты сгорания теряется водород, который входит в состав галогенводородов | Проверяйте себя на предмет того, чего больше: молекул или атомов. Не увлекайтесь чрезмерным округлением. Помните о записи структурных формул |
Общие рекомендации:
- расчет по уравнению реакций обязательно выполняйте в МОЛЯХ, иначе решение задачи не будет зачтено;
- выполняйте хотя бы часть задания: в этом случае у вас есть шанс заработать хоть несколько дополнительных баллов;
- записывайте ответы максимально разборчиво, чтобы не потерять баллы из-за небрежности.
edunews.ru
Как запомнить термины к экзамену ЕГЭ по химии. Советы!
Проверенные советы, которые действительно помогут вам лучше запомнить термины по химии и сдать экзамен ЕГЭ.
Как запомнить термины по химии
Изучая такую науку, как химия, нужно потратить достаточно времени перед экзаменом ЕГЭ, чтобы убедиться, что вы можете правильно пользоваться терминологией, которую учили в течении всего курса. Главная проблема в том, что большинство терминов достаточно трудно запомнить.
Однако, применив немного изобретательности, можно быстрее понять язык химии, биологии или физики. Всегда можно найти связь, если её искать.
Создать запоминающиеся образы для любых технических терминов очень легко. Потратьте немного времени во всем повторении материала, чтобы создать собственный список запоминающихся образов для главных терминов, которые необходимы на экзамене.
Несколько примеров:
Элементы содержат только один вид атомов. Их нельзя расщепить на более простые вещества.
Сложные соединения
Это сложные вещества, состоящие из атомов двух или более различных химических элементов, объединенных хим. связью. Могут расщепляться на более простые. Подумайте о загоне для животных, в котором живут несколько видов.
Кислоты – это вещества, которые:
1) Превращают синюю лакмусовую бумажку в красную. Представьте себе милиционера в синей форме, краснеющего от злости.
2) Кислые на вкус: представьте себе вкус уксуса.
3) При взаимодействии с металлами образуют соли: представьте себе членов тяжелой металл-группы, играющих на «кислой» домашней вечеринке и превращающиеся в столбы из соли.
4) Нейтрализуют основания (базы): бас-гитара нейтрализована.
Сплавами называют любые однородные системы, образованные сплавлением металлов, неметаллов, оксидов, органические в-тв и т.д., и закрепления полученной смеси. Латунь, например, это сплав из меди и цинка. Подумайте о том, как несколько человек сплавляются на плотах.
Это происходит, когда вещество впитывает влагу или воду и растворяется, образуя раствор. Чтобы запомнить это, представьте, как ваш любимый шербет, который слишком долго простоял в шкафу на кухне, превратился в жидкую массу.
Эфлоресценция
Это происходит, когда кристаллическое вещество превращается в порошок под воздействием воздуха или когда соль выходит на поверхность вещества и кристаллизируется. Представьте себе флуоресцентный поток, в котором содержаться растворенные кристаллы, высыхающие на воздухе и превращающиеся в порошок.
Алкоголь состоит из углерода, водорода и кислорода. Это можно запомнить, если подумать об алкоголе следующее: «Купил, выпил, упал», или алкоголь, содержащийся в напитках, произведён путём брожения сахара и дрожжей.
Ионы – это частицы, которые переносят электрический заряд. Они могут (+) заряженные и (-) заряженные. Подумайте о положительных и отрицательных шпионах.
Это (-) заряженные ионы. Подумайте о девушке Ане, сражающейся с вражеским шпионом.
Это (+) заряженные ионы. Подумайте о катящейся шаровой молнии.
Экзотермические реакции
Это хим. реакции, при которых будет выделение теплоты. Подумайте о жарких экзотических странах.
Эндотермические реакции
Это хим. реакции, происходящие с поглощением теплоты из окружающей среды. Подумайте о том, как теплота внедряется.
Аллотропия — это существование химических элементов в виде двух или более простых веществ или форм. Например, у углерода есть несколько абсолютно разных аллотропных форм, включая графит и алмаз. Подумайте о том, как в лесу по тропинкам бродят разные животные. Это хороший пример того, как можно создать индивидуальные ассоциации, столкнувшись с термином или фразой, которые не имеют ничего общего со своим значением или определением.
Аммиак — бесцветный газ с резким удушливым запахом — получают под давлением из водорода и азота в пропорции 3:1. Используя систему ДОМИНИК, представьте, как Кролик и Алиса (КА=31) сжимают два газа вместе. Затем газ преобразуют с помощью процесса Габера и используют в производстве азотной кислоты и удобрений, аммониевых солей, синильной кислоты, взрывчатки, чистящих средств и пластика. Чтобы запомнить это все, представьте себе, что в вашем гардеробе хранятся нижеперечисленные вещи. Боеприпасы напомнят о взрывах и фейерверках, хлорка и сода – о необходимости произвести уборку, а удобрения – о комнатных цветах.
Видите как легко создать нелепые образы, которые останутся в памяти до экзамена. Вам не придется прерываться во время ответа, лихорадочно вспоминая определение: информацию легко будете пересказывать и быстро отвечать на вопросы.
xn--80aakeqfhfoqvpv.xn--p1ai