Схема строение атома мышьяка – Строение атома мышьяка (As), схема и примеры
- Комментариев к записи Схема строение атома мышьяка – Строение атома мышьяка (As), схема и примеры нет
- Советы абитуриенту
- Химик.ПРО – Электронная конфигурация атома элемента (мышьяк)
- Валентность мышьяка (As), формулы и примеры
- пожалуйста, помогите! опишите свойсва мышьяка, исходя из положения его в периодической системе и строении атома.
- Мышьяк, строение атома – Справочник химика 21
- Строение атома ртути (Hg), схема и примеры
- Мышьяк электронное строение – Справочник химика 21
- Что такое мышьяк? Характеристика, свойства и применение
Химик.ПРО – Электронная конфигурация атома элемента (мышьяк)
Напишите электронную конфигурацию атома элемента по указанным координатам в периодической системе: 4 периоде, VA-группе. Изобразите схемы распределения электронов незавершенных подуровней. Определите химические свойства атома.
Решение задачи
4-й период, VA-группа.
Определим, атом какого элемента расположен в 4 периоде, VA-группе Периодической системы Д.И. Менделеева (смотри таблицу Менделеева) – мышьяк (As).
Число электронов в атоме равно заряду его ядра, следовательно, электронная оболочка As содержит 33 электрона. Номер периода равен числу энергетических уровней в атоме, а номер группы – числу электронов на внешнем уровне (валентных электронов). Координаты As: (4, VА) то есть атом имеет четыре энергетических уровня; имеет пять электрон на внешнем уровне; р – элемент.
Запишем электронную конфигурацию атома элемента As:
Используя электронную конфигурацию атома элемента,
Электронная конфигурация атома элемента. Определим химические свойства атома As.
Химические свойства атома определяются строением внешнего энергетического уровня. Вступая в химическое взаимодействие, любой атом стремится завершить внешний уровень. Атом As имеет 5 валентных электронов, поэтому завершение внешнего уровня возможно за счет присоединения трех электронов. Принимая их, атом мышьяка проявляет окислительные свойства:
As0 + 3 e–= As -3
As0 (4s2 4p3)
As -3 (4s2 4p6)
Атом мышьяка может проявлять восстановительные свойства, отдавая электроны внешнего уровня – три или все пять:
As0 – 3 e –= As +3
As0 – 5 e–= As +5
As0 (4s2 4p3)
As +3 (4s2)
As +5 (3s2 3p6 3d10)
Похожие задачи по химии
himik.pro
Валентность мышьяка (As), формулы и примеры
Общие сведения о валентности мышьяка
Мышьяк существует в виде нескольких аллотропных модификаций. Наиболее устойчив при обычных условиях металлический (серый) мышьяк. Он образует серо-стальную хрупкую кристаллическую массу с металлическим блеском на свежем изломе. Плотность 5,72 г/см3. При нагревании под нормальным давлением серый мышьяк сублимируется. Обладает металлической электрической проводимостью.
При быстром охлаждении пара, состоящего из молекул As4, образуется неметаллическая модификация желтый мышьяк. Плотность 2,0 г/см
Валентность мышьяка в соединениях
Мышьяк – тридцать третий по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в четвертом периоде в VA группе. В ядре атома мышьяка содержится 33 протона и 42 нейтрона (массовое число равно 75). В атоме мышьяка есть четыре энергетических уровня, на которых находятся 33 электрона (рис. 1).
Рис. 1. Строение атома мышьяка.
Электронная формула атома мышьяка в основном состоянии имеет следующий вид:
1s22s22p63s23p63d104s24p3.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
Наличие трех неспаренных электронов свидетельствует о том, что мышьяк способен проявлять валентность III (низшая валентность) в своих соединениях (As 2O3, AsH3, HAsO2, H3AsO3).
Для атома мышьяка характерно наличие возбужденного состояния из-за того, что орбитали 4d-подуровня являются вакантными (на четвертом энергетическом слое помимо 4s- и 4p-подуровней есть еще и 4d-подуровень). Электроны 4s-подуровня распариваются и занимают свободную орбиталь 4p -подуровня:
Наличие пяти неспаренных электронов в возбужденном состоянии свидетельствует о том, что мышьяк также проявляет в своих соединениях валентность V (H3AsO4, As2O5) (высшая валентность).
Примеры решения задач
ru.solverbook.com
пожалуйста, помогите! опишите свойсва мышьяка, исходя из положения его в периодической системе и строении атома.
МЫШЬЯК, As (arsenicum), химический элемент VA подгруппы периодической системы элементов, относится к семейству азота N, P, As, Sb, Bi. Мышьяк наиболее известен из-за использования его и его соединений в качестве яда. В рудах встречается в виде сульфидов, арсенидов, арсенитов и арсенатов. Наибольшее распространение среди мышьяксодержащих минералов имеет арсенопирит (мышьяковый колчедан) FeAsS – основное сырье для получения мышьяка, содержащее до 46% As. Лидерами по производству мышьяка являются Франция, Мексика, Швеция и США.Соединения мышьяка известны с античных времен, наиболее ранние сведения встречаются в работах древнегреческого философа Теофраста (372–287 до н. э.) . Открытие элемента обычно приписывают Альберту Великому (Магнусу, 1206–1280), немецкому философу и автору работ по физике. В 1733 Г. Брандт установил, что белый мышьяк в действительности является оксидом мышьяка, а в 1817 шведский химик и минеролог Й. Берцелиус определил относительную атомную массу мышьяка.
Свойства и соединения. Мышьяк относится к неметаллам, хотя из трех его аллотропных модификаций (желтой, черной и металлической, или серой) серая представляет собой кристаллическую массу с металлическим блеском на свежем изломе и, в отличие от других модификаций, обладает металлической электрической проводимостью. Серая форма наиболее стабильна при комнатной температуре и свойства в таблице приведены для нее.
СВОЙСТВА СЕРОГО МЫШЬЯКА
Атомный номер 33
Атомная масса 74,9216
Изотопы
стабильные 75
нестабильные 70–74, 76–79, 81
Температура плавления, ° С 817 (при 37 атм)
Температура кипения, ° С 615 (сублимация)
Плотность, г/см3 5,73
Твердость (по Моосу) 3,5
Содержание в земной коре, % (масс. ) 0,0005
Степени окисления –3, +3, +5
Мышьяк и все его соединения очень ядовиты. Мышьяк не растворяется в воде, на воздухе медленно окисляется, при сильном нагревании сгорает с образованием оксида As2O3 («белый мышьяк» с характерным чесночным запахом, плохо растворяется в воде, но взаимодействует с ней с образованием амфотерного гидроксида мышьяка (III) As(OH)3, или ортомышьяковой кислоты h4AsO3, которая в свободном состоянии не получена, а известна лишь в водном растворе, где находится в равновесии с метамышьяковистой кислотой: . При взаимодействии As2O3 со щелочами образуются соли мышьяковистой кислоты – арсениты).
otvet.mail.ru
Мышьяк, строение атома – Справочник химика 21
Соединения бора с другими элементами. Существует много других типов соединений, в которых атом бора связан с азотом, фосфором, мышьяком, серой и углеродом. Борорганические соединения уже упоминались в разд. 12.5. Здесь мы отметим лишь некоторые соединения бора с азотом. Фрагмент —ЫН — ВК — идентичен структурному элементу—СН = СН—и может замещать его во многих соединениях. Мы уже отмечали графитоподобное строение нитрида бора ВЫ (разд, 12.2). Эту аналогию можно сделать более понятной, если принять, что истинное электронное распределение в связи В — N может быть описано резонансным гибридом,Диапазон геометрических структур, для описания которых полезно обращаться к многогранникам, чрезвычайно широк. Так, например, правильный тетраэдр симметрии одинаково подходит как для молекулы тетрамера мышьяка, Аз4, так и для молекулы метана, СН (рис. 3-27). Однако в их строении имеется одно существенное различие. Оно состоит в том, что в молекуле все четыре атомных ядра, входящих в ее состав, расположены в вершинах правильного тетраэдра, ребрами которого служат химические связи между атомами мышьяка. В молекуле же метана имеется центральный атом углерода, от которого четыре химические связи направлены к четырем вершинам тетраэдра, где находятся атомы водорода. В данном случае ребра тетраэдра уже не являются химическими связями. [c.119]
На основании приведенных данных можно считать твердо установленным экстремум значений проводимости, магнитной восприимчивости, плотности и микротвердости у стекол системы мышьяк—селен, содержащих 9 ат. % мышьяка. Наличие экстремальных значений характеристических величин свидетельствует о существенном изменении структуры стеклообразных сплавов в этой области составов. Л инимальное значение магнитной восприимчивости у стекол, содержащих -9ат. % мышьяка, связано с изменением степени деформации валентных электронных облаков в химических связях As—Se и Se—Se. Это изменение обусловлено статистическим распределением трехмерных пространственных структурных единиц образующегося AsaSes в структуре стеклообразного селена. В таких стеклообразных сплавах с максимально неупорядоченным строением затрудняется сквозной перенос носителей заряда, для них получены заниженные значения плотности и микро-твердости. Перенос носителей заряда с конца оборванной цепи на соседнюю цепь в таких стеклообразных сплавах требует преодоления значительного активационного барьера. Такой перенос может осуществляться в результате перекрытия электронных орбит в процессе низкочастотных термических колеба-
Общим для трех исследованных систем является наличие области максимальных значений парамагнетизма Ван-Флека. Для составов с максимальными значениями парамагнитной составляющей получены также экстремальные значения парамет-)0Б электропроводности и других физико-химических величин. 4з анализа полученных экстремальных значений следует, что стекла указанных составов характеризуются статистическим распределением структурных единиц АзЗез/г, АзЗз/г и ОеЗе4/г в полимерных цепях и циклах стеклообразных селена и серы. Такое распределение приводит к нарушению правильности чередования структурных единиц, нарушению исходного ближнего порядка и вносит тем самым дополнительную асимметрию в строение электронных оболочек атомов. Стекла в системе Аз—Зе с содержанием 9 ат. % мышьяка, в системе Аз—3 с содержанием мышьяка 12 ат. % и в системе Се—Зе с содержанием 6—7 ат, % германия имеют наименьшую степень [c.73]
К химии отравляющих веществ можно применить аналогичные теоретические представления. И здесь, при рассмотрении состава и строения О. В., часто можно подметить группировки атомов, наличие которых определяет общий характер действия данного О. В. Эти группы, по аналогии с теорией красителей, можно назвать токсофорами . Типичнейшим токсофором, является, например, ненасыщенный (трехвалентный) атом мышьяка, атом серы или двухвалентный углерод. [c.31]
Строение элементов. Только азот способен образовывать двухатомные молекулы с =5 М тройной связью. Их большая устойчивость доказывает наличие очень большого взаимного перекрывания обеих р-орбиталей, участвующих в образовании связей. В случае фосфора, мышьяка и сурьмы известны как молекулы тетраэдрической структуры (Р4, Аб4 и 5Ь4) с постепенно уменьшающейся устойчивостью, так и металлические структуры. Висмут существует только в металлическом состоянии. Во всех этих структурах каждый атом соединен тремя простыми связями (ст-связи) с тремя идентичными атомами (см. рис. 128 и 129, стр. 427). Металлические мышьяк, сурьма и висмут изоморфны и образуют бесконечные слоистые решетки, в которых каждый атом имеет трех ближайших соседей (с которыми он связан ковалентно) и трех более удаленных соседей (см. рис. 131, стр. 443). Различие между этими двумя типами соседних атомов уменьшается от Аз к В1, т. е. по мере усиления металлического характера элементов (см. стр. 451 и 454).
Пять комплексных анионов AsO , AsOsS -, ASO2S2 AsOSl и A S -имеют одинаковое строение атом мышьяка находится в центре тетраэдра, а по углам его расположены четыре атома — кислорода или серы. [c.482]
Стекла с содержанием 25 ат. % мышьяка (Аз5з и близкие по составу) имеют цепочечное строение. [c.59]
Наибольшее влияние оказывает таллий на термическую устойчивость и микротвердость стеклообразного АзгЗез, имеющего трехмерное пространственное строение. Термическая устойчивость стекол А58е1,5Т1у, содержащих – 28 ат. % таллия, понИ жается почти на 40%, а микротвердость на 30% по сравнению со стеклообразным триселенидом мышьяка. [c.193]
При этих процессах изомеризации, которые имеют обратимый характер, атом серы (или соответственно мышьяка или азота) восстанавливается или окисляется лишь за счет изменения строения молекулы, т. е. изменения порядка взаимной связи имевшихся в молекуле атомов. При этом приобретение или потеря электронов этим атомом изомеризующейся части молекулы (серы в сульфогруппе или в эфирно группе, мышьяка в арсоногруппе или в эфирной группе и азота в нитрогруппе или в эфирной группе)
chem21.info
Строение атома ртути (Hg), схема и примеры
Общие сведения о строении атома ртути
Относится к элементам d-семейства. Металл. Обозначение – Hg. Порядковый номер – 80. Относительная атомная масса – 200,592 а.е.м.
Электронное строение атома ртути
Атом ртути состоит из положительно заряженного ядра (+80), внутри которого есть 80 протонов и 120 нейтронов, а вокруг, по шести орбитам движутся 80 электронов.
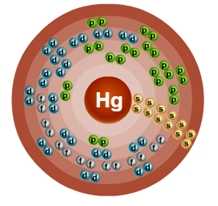
Рис.1. Схематическое строение атома ртути.
Распределение электронов по орбиталям выглядит следующим образом:
+80Hg)2)8)18)32)18)2;
1s22s22p63s23p63d104s24p64f145s25p65d106s2.
Валентными электронами атома золота считаются электроны, расположенные на 5d— и 6s— подуровнях. Энергетическая диаграмма основного состояния принимает следующий вид:
Валентные электроны атома золота можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
6 |
0 |
0 |
+1/2 |
|
s |
6 |
0 |
0 |
-1/2 |
|
d |
5 |
2 |
-2 |
+1/2 |
|
d |
5 |
2 |
-1 |
+1/2 |
|
d |
5 |
2 |
0 |
+1/2 |
|
d |
5 |
2 |
+1 |
+1/2 |
|
d |
5 |
2 |
+2 |
+1/2 |
|
d |
5 |
2 |
-2 |
-1/2 |
|
d |
5 |
2 |
-1 |
-1/2 |
|
d |
5 |
2 |
0 |
-1/2 |
|
d |
5 |
2 |
+1 |
-1/2 |
|
d |
5 |
2 |
+2 |
-1/2 |
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Мышьяк электронное строение – Справочник химика 21
Фосфор, мышьяк или сурьма (имеющие электронное строение внешнего энергетического уровня s pЗ и проявляющие валентность 5), будучи введенными в кристаллические решетки германия или олова (электронное строение внешнего уровня 5 р валентность 4) ведут себя как донорные примеси, т. е. отдают электроны и создают проводимость п-типа. Если же в германий или кремний ввести бор, алюминий, галлий или индий (электронное строение внешнего уровня 5 р, валентность 3), то атомы примеси захватывают четвертый электрон и полупроводник обнаруживает проводимость р-типа. [c.186]Научные работы посвящены физикохимии флотационных процессов и исследованию комплексооб-)азования парамагнитных ионов. Исследовал продукты взаимодействия реагентов с минералами с применением методов радиоспектроскопии. Установил влияние электронно-дырочных центров минералов на изменение их флотационных свойств. Разработал синтез спин-меченых флотореагентов и нашел пути их широкого использования для изучения механизма взаимодействия реагентов с поверхностью минералов. Разработал технологию комплексной переработки руд ряда месторождений. Изучал комнлексообразование парамагнитных ионов с лигандами, содержащими атомы серы, кислорода, азота, селена, фосфора и мышьяка. Установил строение и параметры химической связи ряда комплексов. Разработал способ [c.472]
Электронное строение атомов фосфора, мышьяка, сурьмы и висмута [c.275]
На основании электронного строения атомов р-элементов IV и V групп, изменения их атомных радиусов, их металлических и неметаллических свойств решите вопрос об изменении наиболее устойчивой степени окисления этих элементов по группам. Ответ мотивируйте составлением уравнений реакций растворения в азотной кислоте а) углерода, кремния, олова, свинца б) мышьяка, сурьмы, висмута. [c.67]
Строение внешней электронной оболочки атома Азот Фосфор Мышьяк Сурьма Висмут [c.427]
Рассмотренное строение двойного слоя характерно для собственных полупроводников, в которых нет ни объемных примесей (добавок), ни так называемых поверхностных состояний, обусловленных чаще всего адсорбцией чужеродных атомов. Часто полупроводник в качестве примеси содержит атомы такого вещества, благодаря которому резко увеличивается число свободных электронов п. Такие добавки называются донорами электронов. Для германия такой добавкой служит мышьяк. Поскольку произведение пр в присутствии доноров электронов остается постоянным [уравнение (28.3)1, то увеличение п приводит к соответствующему уменьшению числа дырок р–=К 1п. Поэтому проводимость таких примесных полупроводников п-типа осуществляется в основном за счет свободных электронов в зоне проводимости. Если же атомы примеси резко увеличивают число дырок в валентной зоне, то растет дырочная проводимость и соответственно уменьшается число свободных электронов п = Кз/р- Такого рода примеси называются акцепторами электронов, а полупроводники с дырочной проводимостью — полупроводниками /7-типа. Акцепторами электрона для германия служат атомы галлия. В присутствии примесей соотношение (28.2) в объеме полупроводника уже не остается справедливым. Вместо него следует записать [c.141]
Рассмотренное строение двойного слоя характерно для собственных полупроводников, в которых нет ни объемных примесей (добавок), ни так называемых поверхностных состояний, обусловленных чаще всего адсорбцией чужеродных атомов. Часто полупроводник в качестве примеси содержит атомы такого вещества, благодаря которому резко увеличивается число свободных электронов п. Такие добавки называются донорами электронов. Для германия такой добавкой служит мышьяк. Поскольку произведение пр в присутствии доноров электронов остается постоянным [уравнение (28.3)1, то увеличение п приводит к соответствующему уменьшению числа дырок р = Поэтому [c.150]
Больщинство известных химических элементов, находясь в виде простых веществ, представляют собой металлы. Некоторые элементы (германий, мышьяк, сурьма, алюминий) в одних условиях ведут себя как металлы, в других условиях — как неметаллы. Все металлы имеют на внешнем энергетическом уровне небольшое число валентных электронов — электронные конфигурации металлов представлены в табл. I. Повторение химических свойств металлов обусловлено периодическим повторением строения электронных конфигураций внешних электронных уровней. [c.317]
Сурьма принадлежит к пятой группе периодической системы химических элементов Д. И. Менделеева и входит в подгруппу мышьяка. Атомная масса сурьмы равна 121,75 [213, 992], атомный номер 51. Строение электронной оболочки 1 , 2 , 2/) , З , Зр 45 , 4р , 4 1 , 5s 5р [c.7]
Процессы старения и связанные с ними изменения формы и строения коллоидных частиц в золях сернистого мышьяка протекают очень медленно. Так, золи полуторагодичной давности дают такую же электронографическую картину, как и свежеприготовленные золи. Электронно-микроско-пическая картина отличается лишь тем, что в старых золях можно наблюдать большее количество агрегатов. [c.171]
Внутреннее строение атома В1 роднит его не только с мышьяком и сурьмой, что естественно, но и со многими другими металлами. В атоме висмута есть предпоследний 18-электронный слой (слой типа купро ), который характерен для свинца, а также меди и ее аналогов (Ап, Ag). Интересно, что с этими же элементами висмут нередко бывает связан в рудных месторождениях. [c.240]
Мышьяк Аз (5-10 %), сурьма 8Ь (110″ %) и висмут В1 (2-10″ %). Строение электронных оболочек атомов этих элементов отличается от такового для азота и фосфора. Второй снаружи энергетический уровень в атомах мышьяка, сурьмы и висмута содержит 18 электронов (п—1)5 (тг—1)р (/г—1) 1 . В связи со значительным ростом радиусов атомов и уменьшением энергии ионизации атомы этих элементов могут превращаться в положительно заряженные ионы Однако восстановительные свойства их [c.364]
Соединения бора с другими элементами. Существует много других типов соединений, в которых атом бора связан с азотом, фосфором, мышьяком, серой и углеродом. Борорганические соединения уже упоминались в разд. 12.5. Здесь мы отметим лишь некоторые соединения бора с азотом. Фрагмент —ЫН — ВК — идентичен структурному элементу—СН = СН—и может замещать его во многих соединениях. Мы уже отмечали графитоподобное строение нитрида бора ВЫ (разд, 12.2). Эту аналогию можно сделать более понятной, если принять, что истинное электронное распределение в связи В — N может быть описано резонансным гибридом, [c.291]
Таким образом, теория Льюиса объясняет кислотно- и основные свойства веществ с позиции их строения. Это является одним из существенных недостатков рассматриваемой теории. Не только строение, но и состав и многие другие, неучитываемые Льюисом факторы, определяют проявление веществом кислотно-основного характера. Теория Льюиса не объясняет кислотные свойства многих кислот (в том числе как содержащих, таки не содержащих в своем составе водород), ограничиваясь узкими рамками кислотноосновных реакций, которые протекают по донорно-акцепторному механизму. Например, сопоставляя электронные формулы молекул аммиака и хлорида мышьяка(П1) [c.136]
Строение внешних электронных слоев ионов подгруппы мышьяка такое же, как и катионов подгруппы меди. К подгруппе мышьяка относятся ионы, имеющие а) внешний 18- или (18 + 2)-электронный слой б) незаконченный, т. е. переходный, от 8-к 18-электронному внешнему слою, при условии, если имеются 18- или 32-электронные глубинные слои, наличие которых усиливает и поляризующее действие и собственную поляризуемость ионов. [c.397]
Подгруппа мышьяка. Мышьяк. Элементы подгруппы мышьяка — мышьяк, сурьма и висмут — имеют во внешнем квантовом слое атомов такое же число электронов, как азот и фосфор. Однако они отличаются строением предпоследнего квантового слоя, который содержит 18 электронов . Этим объясняется зна- [c.274]
Свойства атомов. Сопоставление внутренних электронных остовов, валентных и вакантных подуровней показывает, что различия в физических и химических свойствах элементов обусловлены в основном особенностями строения электронных оболочек атомов (табл. 19.2). Атомы элементов этой подгруппы имеют совпадающие по строению валентные подуровни (пз пр ), различные электронные остовы и вакантные подуровни. Два электрона валентных з-подуровней спарены, три электрона р-подуровней заселяют орбитали этих подуровней по одному. Электронная структура азота выделяется отсутствием вакантных подуровней, энергетически близких к наполовину заполненному 2р-подуровню. У фосфора есть один вакантный с -подуровень, а мышьяк, сурьма и висмут имеют несколько вакантных подуровней, близко расположенных к валентным подуровням. [c.383]
Используя представления о кайносимметрии, можно выделить более тонкий вид электронной аналогии, так называемую слоевую аналогию (в дополнение к групповой и типовой аналогии). Слоевыми аналогами называют элементы, которые являются типовыми аналогами, но не имеют внешних или предвнешних кайносимметричных электронов. К таким аналогам относятся, например, в IA-группе К, Rb, s и Fr, а Li и Na не являются слоевыми аналогами с остальными щелочными металлами, поскольку у Li присутствует внешняя кайносимметричная 2р-оболочка (вакантная), а у Na кайносимметрнчная заполненная 2р-оболочка является предвнеш-ней. В ПА-группе слоевыми аналогами являются щелочно-земельные металлы (подгруппа кальция), а в П1А-группе — элементы подгруппы галлия и т. д. С точки зрения электронного строения слоевые аналоги являются между собой полными электронными аналогами. Поэтому рассматривать химические свойства элементов группы мы будет в такой последовательности первый типический элемент, второй типический элемент, остальные элементы главной подгруппы, элементы побочной подгруппы. Например, в И1 группе отдельно рассматриваются бор, алюминий, подгруппа галлия, подгруппа скандия в V группе — азот, фосфор, подгруппа мышьяка, подгруппа ванадия п т. п. [c.15]
Валентная электронная конфигурация всех элементов VA-группы— ns np , т. е. на внешнем энергетическом (валентном) уровне они содержат 2 спаренных s-электрона и 3 неспаренных (в соответствии с правилом Гунда) электрона на трехкратно вырожденном р-уровне. Однако между элементами этой группы существуют и различия в электронном строении. Так, у фосфора в отличие от азота впервые появляется вакантный внешний М-уровепь, что обусловливает возможность промотирования одного 35-электрона с образованием пятиковалентного состояния, которое, как известно, отсутствует у азота. У мышьяка, сурьмы и висмута к вакантному -уровню добавляется еще в отличие от фосфора полностью завершенный внутренний (п—1) -уровень, а у висмута, следующего за лентаноидами, кроме того, и 4/ -уровень. [c.282]
Наличие заполненных предвнешних (п—l)d- и (п—2)/-уровней сверх оболочки предыдущего благородного газа накладывает отпечаток на свойства элементов подгруппы мышьяка. Отметим, что между собой мышьяк, сурьма и висмут являются полными электронными аналогами и отличаются с точки зрения электронного строения от типических элементов VA-группы — азота и фосфора, т. е. по отношению к ним являются неполными электронными аналогами. [c.282]
Подгруппа иьппьяка. Характеристика элементов УА-группы. Валентная электронная конфигурация всех элементов УА-Г1зуппы — пз пр , т.е. на внешнем энергетическом (валентном) уровне они содержат два спаренных -электрона и три неспаренных электрона на трехкратно вырожденном пр-уровне. Однако между элементами этой группы существуют и р личия в электронном строении. У мышьяка, сурьмы и висмута к вакантному пс(-уровню добавляется еще в отличие от фосфора полностью завершенный внутренний (п — 1) -уровень, а у висмута, следующего за лантаноидами, кроме того, и 4/ -уровень. В силу наличия внутренних и /оболочек, экранирующих внешние электроны, в ряду Аз — 8Ь — В1 проявляется вторичная периодичность. В результате этого для среднего элемента ряда — сурьмы — степень окисления +5 оказывается более стабильной, чем для мышьяка и висмута. [c.417]
В результате оба атома образуют ковалентные а-связи с тремя заместителями, например КзАз или Кз5Ь, причем орбитали центрального атома оказываются средними между Зр-орби-талями, требующими угла 90° между связями, и хр -гибридизо-ванными орбиталями, требующими углов около 109,5° [1]. Как и следовало ожидать из электронного строения и по аналогии с такими же соединениями фосфора, соединения трехвалентного мышьяка и сурьмы являются основаниями Льюиса и образуют четвертичные соли. [c.302]
Хотя химия органических соединений фосфора и мышьяка широко изучается многими авторами с использованием разнообразных физических и химических методов /1-15/,проблема механизма электронных взаимодействий в них еще далека от своего решения.С целью получения дополнительной информации по этому вопросу в настоящей работе исследовано влияние факторов электронного строения на скорость основного дейтерообмена метильной группы и некоторые спектроскопические характеристики третичных метил-фенилфосфинов и арсинов,соответствующих им окисей,сульфидов и “ониевых” соединений. [c.443]
Свойства элементов и простых веществ закономерно изменяются в подгруппе с ростом радиуса атомов и уменьшением энергии ионизации, как это можно видеть из табл. 27. Азот и фосфор — типичные неметаллы, т. е. кислотообразователи. Различия в строении предвнеш-него электронного уровня у атомов фосфора и мышьяка меньше сказываются на изменении свойств элементов, чем при переходе от кремния к германию в IVA-подгруппе. У мышьяка сильнее выражены неметаллические свойства. У сурьмы неметаллические и металлические свойства проявляются приблизительно в одинаковой степени. Для висмута характерно преобладание металлических (основных) свойств. [c.339]
Бинарные соединения, оба компонента которых расположены справа от границы Цинтля, как отмечено выше, характеризуются преимущественно ковалентным типом взаимодействия в силу незначительной разности ОЭО. Правило октета здесь соблюдается, поскольку число валентных электронов у обоих компонентов достаточно для реализации ковалентного взаимодействия. Для соединений, подчиняющихся правилу формальной валентности, у катионообразователя необходимо учитывать лишь число электронов, участвующих в образовании связи. Так, в оксидах мышьяка АзгОз и АззОз у кислорода в обоих случаях учитывается шесть электронов, а у мышьяка в первом случае три, а втором — пять электронов. Тогда для АзгОз получим (3-2 + 6-3)/3 = 8, а для АзгОб — (5-2 + 6-5)/5 = 8. Если соединения не подчиняются правилу формальной валентности, то применимо правило Музера — Пирсона. Особенности кристаллохимического строения бинарных соединений с компонентами, расположенными справа от границы Цинтля, состоят в том, что в их структуре присутствуют группировки атомов в виде цепочек, сеток и молекул. Следовательно, кроме ковалентной связи здесь реализуется и межмолекулярное взаимодействие. [c.261]
В настоящей работе было предпринято электронно-микроскопическое исследование структуры некоторых аморфных полимеров, обладающих различным строением молекулярных цепей. В качестве объектов были изучены полимеры мышьяка (сальварсан), полиакриламид и сополимер па основе метилметакрилата и метакриловой кислоты. Таким образом, были исследованы полимеры, содержащие различные полярные группы в цепи и, следовательно, обладающие различными внутри- и межмолекулярными силами взаимодействия. [c.121]
Проведены некоторые определения сравнительной легкости, с которой фосфины, арсины и стибины аналогичного строения способны расширять свою валентную оболочку. Обширная информация получена при использовании этих соединений в качестве лигандов в комплексах с металлами. Чатт и Харт [11] исследовали монозамещенные карбонилы никеля Ы1(С0)зЦ где Ь=(СбН5)зР или (СбН5)зАз. Эти соединения были приготовлены вытеснением окиси углерода из тетракарбонила никеля, причем эта реакция шла много быстрее в случае фосфина. Однако частота колебаний карбонильной группы фосфина составляла 2063 см тогда как для арсина 2072 см К На основании этих данных было принято, что обратная подача электронов с заполненных -орбиталей никеля в направлении СО-групп больше в случае фосфинового комплекса по сравнению с тем же эффектом в арсиновом комплексе. Другими словами, арсин (фактически в виде арсониевой группы, поскольку мышьяк поделил электроны с никелем) вновь принимает электроны на свои вакантные -орбитали в большей мере, чем фосфор в фосфине (т. е. вклад структуры Па больше, чем вклад 1а в истинное р ас-пределение электронной плотности в соответствующем комплексе). [c.304]
Как видно из приведенных в табл. III. 4 данных, по химическому строению диазиды делятся на четыре группы к первой группе (соединения 1—6) относятся вещества, в которых азидсодержащие арильные ядра не сопряжены, ко второй (7—20)—соединения, в которых электронное взаимодействие между такими ядрами осуществляется через карбонил, к третьей (21—27)—диазиды, в молекулах которых имеется единая сопряженная система, к четвертой (28—31)—формально сопряженные и несопряженные диазиды, содержащие гетероатом фосфора, мышьяка и другие в цепи, связывающей два ароматических ядра. [c.122]
С)т формы частиц дисперсной фазы зависят некоторые свойства коллоидных растворов. Так, коллоидные системы асимметрического строения способны образовать внутреннюю сетчатую структуру. На рис. 174 и 175 приведены полученные на электронном микроскопе снимки коллоидных частиц свежеприготовленного золя сульфида мышьяка и пятнокиси ванадия. Как видно из этих рисунков, частицы пятиолиси [c.407]
На основании приведенных данных можно считать твердо установленным экстремум значений проводимости, магнитной восприимчивости, плотности и микротвердости у стекол системы мышьяк—селен, содержащих 9 ат. % мышьяка. Наличие экстремальных значений характеристических величин свидетельствует о существенном изменении структуры стеклообразных сплавов в этой области составов. Л инимальное значение магнитной восприимчивости у стекол, содержащих -9ат. % мышьяка, связано с изменением степени деформации валентных электронных облаков в химических связях As—Se и Se—Se. Это изменение обусловлено статистическим распределением трехмерных пространственных структурных единиц образующегося AsaSes в структуре стеклообразного селена. В таких стеклообразных сплавах с максимально неупорядоченным строением затрудняется сквозной перенос носителей заряда, для них получены заниженные значения плотности и микро-твердости. Перенос носителей заряда с конца оборванной цепи на соседнюю цепь в таких стеклообразных сплавах требует преодоления значительного активационного барьера. Такой перенос может осуществляться в результате перекрытия электронных орбит в процессе низкочастотных термических колеба- [c.44]
Общим для трех исследованных систем является наличие области максимальных значений парамагнетизма Ван-Флека. Для составов с максимальными значениями парамагнитной составляющей получены также экстремальные значения парамет-)0Б электропроводности и других физико-химических величин. 4з анализа полученных экстремальных значений следует, что стекла указанных составов характеризуются статистическим распределением структурных единиц АзЗез/г, АзЗз/г и ОеЗе4/г в полимерных цепях и циклах стеклообразных селена и серы. Такое распределение приводит к нарушению правильности чередования структурных единиц, нарушению исходного ближнего порядка и вносит тем самым дополнительную асимметрию в строение электронных оболочек атомов. Стекла в системе Аз—Зе с содержанием 9 ат. % мышьяка, в системе Аз—3 с содержанием мышьяка 12 ат. % и в системе Се—Зе с содержанием 6—7 ат, % германия имеют наименьшую степень [c.73]
Одним из последних экспериментальных подтверждений уменьшения тенденции к образованию я-связей у тяжелых элементов V группы является работа Бигли и др. [23], изучавших молекулу А5(5 Нз)з. Эта молекула имеет пирамидальное строение, все углы SiAsS равны 93°. Очевидно, для образования связей АзЗ мышьяк использует только р-орбитали неподеленная пара электронов располагается в основном на х-орбитали. Электроны неподеленной пары не могут переходить на вакантные З -орбитали кремния и вносить вклад в образование двойных связей. [c.175]
chem21.info
Что такое мышьяк? Характеристика, свойства и применение
Мышьяк – химический элемент группы азота (группа 15 таблицы Менделеева). Это серое с металлическим блеском хрупкое вещество (α-мышьяк) с ромбоэдрической кристаллической решеткой. При нагревании до 600°C As сублимирует. При охлаждении паров возникает новая модификация — желтый мышьяк. Выше 270°C все формы As переходят в черный мышьяк.
История открытия
О том, что такое мышьяк, было известно задолго до признания его химическим элементом. В IV в. до н. э. Аристотель упоминал о веществе под названием «сандарак», которое, как теперь полагают, было реальгаром, или сульфидом мышьяка. А в I веке н. э. писатели Плиний старший и Педаний Диоскорид описывали аурипигмент – краситель As2S3. В XI в. н. э. различались три разновидности «мышьяка»: белый (As4O6), желтый (As2S3) и красный (As4S4). Сам элемент, вероятно, впервые был выделен в XIII веке Альбертом Великим, который отметил появление металлоподобного вещества, когда арсеникум, другое название As2S3, был нагрет с мылом. Но уверенности в том, что этот ученый-естествоиспытатель получил чистый мышьяк, нет. Первое подлинное свидетельство о выделении чистого химического элемента датировано 1649 годом. Немецкий фармацевт Иоганн Шредер приготовил мышьяк, нагревая его оксид в присутствии угля. Позже Никола Лемери, французский врач и химик, наблюдал образование этого химического элемента при нагревании смеси его оксида, мыла и поташа. К началу XVIII века мышьяк уже был известен и как уникальный полуметалл.

Распространенность
В земной коре концентрация мышьяка невелика и составляет 1,5 промилле. Он встречается в почве и минералах и может попасть в воздух, воду и грунт благодаря ветровой и водной эрозии. Кроме того, элемент поступает в атмосферу из других источников. В результате извержения вулканов в воздух выделяется около 3 тыс. т мышьяка в год, микроорганизмы образуют 20 тыс. т летучего метиларсина в год, а в результате сжигания ископаемого топлива за тот же период выделяется 80 тыс. т.
Несмотря на то что As – смертельный яд, он является важной составляющей питания некоторых животных и, возможно, человека, хотя необходимая доза не превышает 0,01 мг/сутки.
Мышьяк крайне трудно перевести в водорастворимое или летучее состояние. Тот факт, что он довольно мобилен, означает, что большие концентрации вещества в каком-то одном месте появиться не могут. С одной стороны, это хорошо, но с другой – легкость, с которой он распространяется, является причиной того, что загрязнение мышьяком становится все большей проблемой. Из-за деятельности человека, в основном за счет добычи и плавки, обычно немобильный химический элемент мигрирует, и сейчас его можно найти не только в местах его естественной концентрации.
Количество мышьяка в земной коре составляет около 5 г на тонну. В космосе его концентрация оценивается как 4 атома на миллион атомов кремния. Этот элемент широко распространен. Небольшое его количество присутствует в самородном состоянии. Как правило, образования мышьяка чистотой 90–98% встречаются вместе с такими металлами, как сурьма и серебро. Большая его часть, однако, входит в состав более чем 150 различных минералов – сульфидов, арсенидов, сульфоарсенидов и арсенитов. Арсенопирит FeAsS является одним из самых распространенных As-содержащих минералов. Другие распространенные соединения мышьяка – минералы реальгар As4S4, аурипигмент As2S3, леллингит FeAs2 и энаргит Cu3AsS4. Также часто встречается оксид мышьяка. Большая часть этого вещества является побочным продуктом выплавки медных, свинцовых, кобальтовых и золотых руд.
В природе существует только один стабильный изотоп мышьяка – 75As. Среди искусственных радиоактивных изотопов выделяется 76As c периодом полураспада 26,4 ч. Мышьяк-72, -74 и -76 используются в медицинской диагностике.

Промышленное производство и применение
Металлический мышьяк получают при нагреве арсенопирита до 650-700 °C без доступа воздуха. Если же арсенопирит и другие металлические руды нагревать с кислородом, то As легко вступает с ним в соединение, образуя легко возгоняемый As4O6, также известный как «белый мышьяк». Пары оксида собирают и конденсируют, и позже очищают повторной возгонкой. Большая часть As производится путем его восстановления углеродом из белого мышьяка, полученного таким образом.
Мировое потребление металлического мышьяка является относительно небольшим – всего несколько сотен тонн в год. Большая часть того, что потребляется, поступает из Швеции. Он используется в металлургии из-за его металлоидных свойств. Около 1% мышьяка применяется в производстве свинцовой дроби, так как он улучшает округлость расплавленной капли. Свойства подшипниковых сплавов на основе свинца улучшаются как по тепловым, так и по механическим характеристикам, когда они содержат около 3% мышьяка. Наличие малого количества этого химического элемента в свинцовых сплавах закаляет их для использования в аккумуляторных батареях и кабельной броне. Небольшие примеси мышьяка повышают коррозионную стойкость и тепловые свойства меди и латуни. В чистом виде химический элементарный As используется для нанесения бронзового покрытия и в пиротехнике. Высокоочищенный мышьяк находит применение в полупроводниковой технике, где он используется с кремнием и германием, а также в форме арсенида галлия (GaAs) в диодах, лазерах и транзисторах.

Соединения As
Так как валентность мышьяка равна 3 и 5, и он имеет ряд степеней окисления от -3 до +5, элемент может образовывать различные виды соединений. Наиболее важное коммерческое значение имеют его оксиды, основными формами которых являются As4O6 и As2O5. Мышьяковистый оксид, широко известный как белый мышьяк, – это побочный продукт обжига руд меди, свинца и некоторых других металлов, а также арсенопирита и сульфидных руд. Он является исходным материалом для большинства других соединений. Кроме того, он используется в пестицидах, служит обесцвечивающим веществом в производстве стекла и консервантом для кож. Пятиокись мышьяка образуется при воздействии окислителя (например, азотной кислоты) на белый мышьяк. Он является основным ингредиентом инсектицидов, гербицидов и клея для металла.
Арсин (AsH3), бесцветный ядовитый газ, состоящий из мышьяка и водорода, – это еще одно известное вещество. Вещество, называемое также мышьяковистым водородом, получают путем гидролиза металлических арсенидов и восстановления металлов из соединений мышьяка в растворах кислот. Он нашел применение как легирующая добавка в полупроводниках и боевой отравляющий газ. В сельском хозяйстве большое значение имеют мышьяковая кислота (H3AsO4), арсенат свинца (PbHAsO4) и арсената кальция [Са3(AsO4)2], которые используются для стерилизации почвы и борьбы с вредителями.
Мышьяк – химический элемент, образующий множество органических соединений. Какодин (СН3)2As−As(СН3)2, например, используется при подготовке широко используемого десиканта (осушающего средства) – какодиловой кислоты. Сложные органические соединения элемента применяются в лечении некоторых заболеваний, например, амебной дизентерии, вызванной микроорганизмами.

Физические свойства
Что такое мышьяк с точки зрения его физических свойств? В наиболее стабильном состоянии он представляет собой хрупкое твердое вещество стального серого цвета с низкой тепловой и электрической проводимостью. Хотя некоторые формы As являются металлоподобными, отнесение его к неметаллам – это более точная характеристика мышьяка. Есть и другие виды мышьяка, но они не очень хорошо изучены, особенно желтая метастабильная форма, состоящая из молекул As4, подобно белому фосфору Р4. Мышьяк возгоняется при температуре 613 °C, и в виде пара он существует как молекулы As4, которые не диссоциируют до температуры около 800 °C. Полная диссоциация на молекулы As2 происходит при 1700 °С.

Строение атома и способность образовывать связи
Электронная формула мышьяка – 1s22s22p63s23p63d104s24p3 – напоминает азот и фосфор в том, что во внешней оболочке есть пять электронов, но он отличается от них наличием 18 электронов в предпоследней оболочке вместо двух или восьми. Добавление 10 положительных зарядов в ядре во время заполнения пяти 3d-орбиталей часто вызывает общее уменьшение электронного облака и увеличение электроотрицательности элементов. Мышьяк в таблице Менделеева можно сравнить с другими группами, которые наглядно демонстрируют эту закономерность. Например, общепризнанно, что цинк является более электроотрицательным, чем магний, а галлий – чем алюминий. Однако в последующих группах эта разница уменьшается, и многие не согласны с тем, что германий электроотрицательнее кремния, несмотря на обилие химических доказательств. Подобный переход от 8- к 18-элементной оболочке от фосфора к мышьяку может увеличить электроотрицательность, но это остается спорным.
Сходство внешней оболочки As и P говорит о том, они могут образовывать 3 ковалентные связи на атом при наличии дополнительной несвязанной электронной пары. Степень окисления должна, следовательно, быть +3 или -3, в зависимости от относительной взаимной электроотрицательности. Строение мышьяка также говорит о возможности использования внешней d-орбитали для расширения октета, что позволяет элементу образовывать 5 связей. Она реализуется только при реакции с фтором. Наличие свободной электронной пары для образования комплексных соединений (через донорство электронов) в атоме As проявляется гораздо меньше, чем у фосфора и азота.
Мышьяк стабилен в сухом воздухе, но во влажном покрывается черным оксидом. Его пары легко сгорают, образуя As2O3. Что такое мышьяк в свободном состоянии? Он практически не подвержен воздействию воды, щелочей и неокисляющих кислот, но окисляется азотной кислотой до состояния +5. С мышьяком реагируют галогены, сера, а многие металлы образуют арсениды.

Аналитическая химия
Вещество мышьяк качественно можно обнаружить в виде желтого аурипигмента, выпадающего в осадок под действием 25% раствора соляной кислоты. Следы As, как правило, определяются путем его преобразования в арсин, который можно обнаружить с помощью теста Марша. Арсин термически разлагается, образуя черное зеркало из мышьяка внутри узкой трубки. По методу Гутцайта пробник, пропитанный хлоридом ртути, под действием арсина темнеет из-за выделения ртути.
Токсикологическая характеристика мышьяка
Токсичность элемента и его производных широко изменяется в значительных пределах, от чрезвычайно ядовитого арсина и его органических производных до просто As, который относительно инертен. О том, что такое мышьяк, говорит применение его органических соединений в качестве боевых отравляющих веществ (люизит), везиканта и дефолианта («Агент блю» на основе водной смеси 5% какодиловой кислоты 26% ее натриевой соли).
В целом производные данного химического элемента раздражают кожу и вызывают дерматит. Также рекомендуется защита от вдыхания мышьяк-содержащей пыли, но большая часть отравлений происходит при его употреблении внутрь. Предельно допустимая концентрация As в пыли за восьмичасовой рабочий день составляет 0,5 мг/м3. Для арсина доза снижается до 0,05 части на миллион. Помимо использования соединений данного химического элемента в качестве гербицидов и пестицидов, применение мышьяка в фармакологии позволило получить сальварсан – первый успешный препарат против сифилиса.

Воздействие на здоровье
Мышьяк является одним из наиболее токсичных элементов. Неорганические соединения данного химического вещества в естественных условиях встречаются в небольших количествах. Люди могут подвергаться воздействию мышьяка через пищу, воду и воздух. Экспозиция может также произойти при контакте кожи с зараженной почвой или водой.
Содержание мышьяка в продуктах питания довольно низкое. Однако его уровни в рыбе и морепродуктах могут быть очень высокими, так как они поглощают данный химический элемент из воды, в которой живут. Значительное количество неорганического мышьяка в рыбе может представлять опасность для здоровья человека.
Воздействию вещества также подвержены люди, которые с ним работают, живут в домах, построенных из обработанной им древесины, и на землях сельскохозяйственного назначения, где в прошлом применялись пестициды.
Неорганический мышьяк может вызывать различные последствия для здоровья человека, такие как раздражение желудка и кишечника, снижение производства красных и белых клеток крови, изменение кожи и раздражение легких. Предполагается, что поглощение значительного количества этого вещества может увеличить шансы развития рака, особенно рака кожи, легких, печени и лимфатической системы.
Очень высокие концентрации неорганического мышьяка являются причиной бесплодия и выкидышей у женщин, дерматитов, снижения сопротивляемости организма инфекциям, проблем с сердцем и повреждений мозга. Кроме того, этот химический элемент способен повредить ДНК.
Смертельная доза белого мышьяка равна 100 мг.
Органические соединения элемента ни рака, ни повреждений генетического кода не вызывают, но высокие дозы могут нанести вред здоровью человека, например вызвать нервные расстройства или боли в животе.
Свойства As
Основные химико-физические свойства мышьяка следующие:
- Атомное число – 33.
- Атомный вес – 74,9216.
- Температура плавления серой формы – 814 °C при давлении 36 атмосфер.
- Плотность серой формы – 5,73 г/см3при 14 °C.
- Плотность желтой формы – 2,03 г/см3 при 18 °C.
- Электронная формула мышьяка – 1s22s22p63s23p63d104s24p3.
- Состояния окисления – -3, +3, +5.
- Валентность мышьяка – 3, 5.
fb.ru